题目内容
7.常温下,下列有关叙述正确的是( )| A. | 饱和氯水中滴加NaOH至溶液呈中性:c(Na+)═2c(ClO-)+c(HClO) | |
| B. | 100ml 0.2mol/L的NH4Cl溶液和200ml 0.1mol/L的NH4Cl溶液所含有的n(NH4+)相同 | |
| C. | pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)≥c(H+) | |
| D. | 常温下,pH=4.75、浓度均为0.1mol/L的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
分析 A.溶液呈中性,则c(H+)=c(OH-),然后结合物料守恒、电荷守恒进行判断;
B.铵根离子的浓度不同,在溶液中的水解程度不同;
C.分别根据该一元酸为强酸和弱酸进行讨论;
D.pH=4.75浓度均为0.1mol•L-1的CH3COOH、CH3COONa混合溶液,说明醋酸的电离程度大于CH3COO-的水解程度,则c(CH3COO-)>c(Na+)>c(CH3COOH),然后结合电荷守恒进行判断.
解答 解:A.溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得:c(H+)+c(Na+)=c(Cl-)+c(Cl0-)+c(OH-),所以c(Na+)=c(Cl-)+c(ClO-),根据物料守恒得:c(Cl-)=c(ClO-)+c(HClO),二者结合可得:c(Na+)=c(HClO)+2c(ClO-),故A正确;
B.100ml 0.2mol/L的NH4Cl溶液和200ml 0.1mol/L的NH4Cl溶液中含有溶质的物质的量都是0.02mol,由于两溶液中铵根离子浓度不同,则铵根离子的水解程度,不同,所以两溶液所含n(NH4+)不相同,故B错误;
C.pH=2的一元酸和pH=12的一元强碱等体积混合,若酸为强酸,则混合液中:c(OH-)=c(H+),若为弱酸,则混合液中酸过量:c(OH-)<c(H+),所以混合液中正确的浓度关系为:c(OH-)≤c(H+),故C错误;
D.pH=4.75浓度均为0.1mol•L-1的CH3COOH、CH3COONa混合溶液,说明醋酸的电离程度大于CH3COO-的水解程度,则:c(CH3COO-)>c(Na+)>c(CH3COOH),根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+)可知:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,涉及酸碱混合的定性判断、离子浓度大小比较、盐的水解原理等知识,明确电荷守恒、物料守恒的含有为解答关键,试题侧重考查学生的分析、理解能力.

 阅读快车系列答案
阅读快车系列答案| A. | 甲烷 | B. | 四氯化碳 | C. | 乙烯 | D. | 苯 |
| A. | 气体的平均相对分子质量不再改变 | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | 单位时间内生成3n mol X,同时生成n mol Y |
| A. | 先配制0.10 mol/L CH3COOH溶液,再测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 | |
| B. | 先配制0.01 mol/L和0.10 mol/L的CH3COOH,再分别用pH计测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质 | |
| C. | 取等体积、等pH的CH3COOH的溶液和盐酸分别与足量锌反应,测得反应过程中醋酸产生H2速率较慢且最终产生H2较多,则可证明醋酸为弱电解质 | |
| D. | 配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质 |
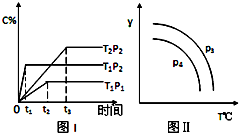 在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)?2C(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )
在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)?2C(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )| A. | 该反应是吸热反应 | |
| B. | x=2 | |
| C. | P3<P4,y轴可表示混合气体的相对分子质量 | |
| D. | P3>P4,y轴可表示C物质在平衡体积中的百分含量 |
| A. | 乙烯合成聚乙烯 | |
| B. | 烯烃与水煤气发生羰基合成反应RCH=CH2+H2+CO$\stackrel{催化剂}{→}$RCH2CH2CHO | |
| C. | 甲烷、CO合成乙酸乙酯2CH4+2CO$\stackrel{催化剂}{→}$CH3COOCH2CH3 | |
| D. | 实验室用乙醇制乙烯 |
| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素周期律的实质是因为元素原子最外层电子数由1→8周期性变化而引起的 | |
| C. | 半径由大到小、氧化性由弱到强的是K+、Mg2+、Al3+、H+,而还原性由弱到强的则是I-、Br-、Cl-、F- | |
| D. | 某元素R的最高价氧化物化学式为R2O5,又知R的气态氢化物中含氢的质量分数为8.8%,则R的相对原子质量为28 |
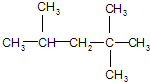 :它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷,若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3;
:它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷,若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3;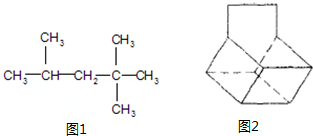
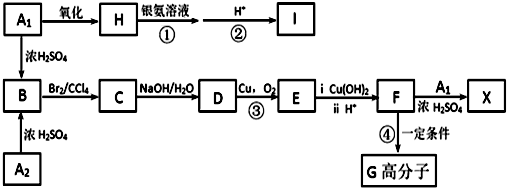
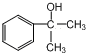 X
X
 ;③2
;③2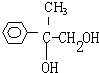 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2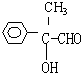 +2H2O
+2H2O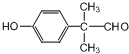 .
.