题目内容
18.下列物质既能与溴水反应又能与酸性高锰酸钾溶液反应的是( )| A. | 甲烷 | B. | 四氯化碳 | C. | 乙烯 | D. | 苯 |
分析 能和溴水反应的物质具有还原性、碳碳不饱和键、醛基或苯环上酚羟基邻对位含有氢原子的酚等,具有还原性的物质、含有不饱和键的有机物、连接苯环的碳原子上含有氢原子的苯的同系物等都能被酸性高锰酸钾溶液氧化,据此分析解答.
解答 解:A.甲烷性质较稳定,和溴、酸性高锰酸钾溶液都不反应,故A错误;
B.四氯化碳性质较稳定,和溴、酸性高锰酸钾溶液都不反应,故B错误;
C.乙烯中含有碳碳双键,性质较活泼,能和溴发生加成反应而使溴水褪色,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故C正确;
D.苯性质较稳定,不能被酸性高锰酸钾溶液氧化,所以不能使酸性高锰酸钾溶液褪色,但苯能萃取溴水中的溴而使溴水褪色,故D错误;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查不饱和烃、饱和烃的性质,明确官能团及其性质是解本题关键,易错选项是D,知道苯能使溴水褪色原理.

练习册系列答案
相关题目
18.Al、Fe、Cu都是重要的金属元素.下列说法正确的是( )
| A. | FeCl2可通过化合反应一步制得 | |
| B. | 不能用稀盐酸区别二氧化锰、氧化铜、还原铁粉三种黑色粉末 | |
| C. | 采用将MgSO4溶液直接蒸干的方法不能制备MgSO4固体 | |
| D. | 可通过电解熔融MgCl2来制取Mg,故也可通过电解熔融的AlCl3来制取Al |
6.全部属于纯净物的组合是( )
| A. | 福尔马林、白酒、食醋 | B. | 汽油、油脂、酚醛树脂 | ||
| C. | 石炭酸、盐酸、冰醋酸 | D. | 甘油、乙醇钠、氯仿 |
13.下列说法正确的是( )
| A. | 乙烯的年产量通常用来衡量一个国家的石油化工发展水平 | |
| B. | 煤的干馏属于物理变化 | |
| C. | 石油裂化的主要目的是除去石油中的杂质 | |
| D. | 压缩天然气和液化石油气的主要成分均为一氧化碳 |
10.一定温度下,在甲、乙、丙三个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示.下列判断中正确的是( )
| 甲 | 乙 | 丙 | ||
| 密闭容器体积/L | 2 | 2 | 2 | |
| 起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率% | 80 | α1 | α2 | |
| A. | 该温度下,甲容器10min达到平衡,平均速率为v(SO3)=0.032 mol•L-1•min-1 | |
| B. | SO2的平衡转化率:α1<80% | |
| C. | 容器中SO3的物质的量浓度:2c(甲)>c(丙) | |
| D. | 甲中反应的平衡常数K为400 |
7.常温下,下列有关叙述正确的是( )
| A. | 饱和氯水中滴加NaOH至溶液呈中性:c(Na+)═2c(ClO-)+c(HClO) | |
| B. | 100ml 0.2mol/L的NH4Cl溶液和200ml 0.1mol/L的NH4Cl溶液所含有的n(NH4+)相同 | |
| C. | pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)≥c(H+) | |
| D. | 常温下,pH=4.75、浓度均为0.1mol/L的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
8.《化学教育》报道了数起因食用有“瘦肉精”的猪肉和内脏,而发生急性中毒的恶性事件.这足以说明,“瘦肉精”变成了“害人精”.“瘦肉精”的结构可表示为:
下列说法正确的是( )

下列说法正确的是( )
| A. | 摩尔质量为313.5 g | B. | 属于芳香烃 | ||
| C. | 分子式为C12H19Cl3N20 | D. | 消去产物有2种 |

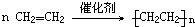 .
.