题目内容
【题目】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______。基态碳原子的核外电子占有______个原子轨道。
(2)光化学烟雾中除了含有NOx外,还含有HCOOH、![]() (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN中C的杂化方式有______。1mol PAN中含有的σ键数目为______。组成PAN的元素的电负性大小顺序为______。
②相同压强下,HCOOH的沸点比CH3OCH3______(填“高”或“低”),
(3)水溶液中有H3O+、![]() 、
、![]() 等微粒的形式。请画出
等微粒的形式。请画出![]() 的结构式:______。
的结构式:______。
【答案】氦 4 sp2 、sp3 10NA(或6.02×1024) O>N>C>H 高 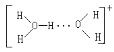
【解析】
判断有机物中C原子的杂化方式可以根据有机物中C的成键方式进行判断;计算![]() 键数目时,要注意一个双键中含有一个
键数目时,要注意一个双键中含有一个![]() 键;比较由分子构成的物质的沸点大小时,可以从摩尔质量,氢键以及结构中支链个数这几个角度入手分析;书写
键;比较由分子构成的物质的沸点大小时,可以从摩尔质量,氢键以及结构中支链个数这几个角度入手分析;书写![]() 的结构时,要清楚其是由水合氢离子与水分子通过氢键形成的。
的结构时,要清楚其是由水合氢离子与水分子通过氢键形成的。
(1)宇宙中氢元素占88.6%、氦占11.1%,宇宙中含量最多的元素是氢和氦;C的电子排布为1s22s22p2,s能级只有1个轨道,p能级有3个轨道,基态原子电子排布满足洪特规则,因此基态碳原子的2p能级有两个轨道被占据,基态碳原子核外电子总计占有4个轨道;
(2)①PAN分子中,C原子形成了单键和双键,形成4条单键的碳原子,其键角约为109°28′,形成一个双键的碳原子,其键角约为120°,因此碳原子的杂化类型有sp3、sp2;一个双键含有一个σ键,由PAN结构可知,一个PAN分子中含有10个σ键,所以1molPAN中含有的σ键数目为10NA;PAN分子中含有C、H、N、O元素,元素的非金属性越强,其电负性越大,则电负性:O>N>C>H;
②由于HCOOH存在分子间氢键,CH3OCH3只存在分子间作用力,所以HCOOH的沸点比CH3OCH3高;
(3)![]() 是由水分子和水合氢离子通过氢键形成的微粒,则
是由水分子和水合氢离子通过氢键形成的微粒,则![]() 的结构式为:
的结构式为:![]() 。
。

 一线名师权威作业本系列答案
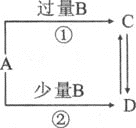
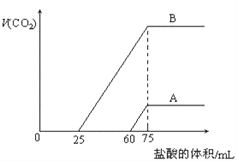
一线名师权威作业本系列答案【题目】将一定量的氨基甲酸置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
A. 在低温下该反应能自发进行
B. 15℃时,该反应的化学平衡常数约为2.0
C. 当混合气体平均相对分子质量不变时,该反应达到化学反应限度
D. 恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变
【题目】镀作为一种新兴材料日益被重视,有“超级金属![]() 尖端金属
尖端金属![]() 空间金属”之称。工业上常用绿柱石
空间金属”之称。工业上常用绿柱石![]() 主要成分
主要成分![]() ,还含有铁等杂质
,还含有铁等杂质![]() 冶炼镀,一种简化的工艺流程如下:
冶炼镀,一种简化的工艺流程如下:
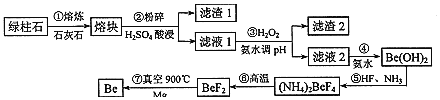
按元素周期表的对角线规则,Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如表。回答下列问题:
|
|
|
| |
开始沉淀时 |
|
|
|
|
沉淀完全时 |
|
|
|
|
![]() 步骤
步骤![]() 中将熔块粉碎的目的是______;滤渣1的主要成分是_____。
中将熔块粉碎的目的是______;滤渣1的主要成分是_____。
![]() 步骤
步骤![]() 加入
加入![]() 时发生反应的离子方程式为______,从滤液1中得到沉淀的合理pH为______
时发生反应的离子方程式为______,从滤液1中得到沉淀的合理pH为______![]() 填序号
填序号![]() 。
。
A![]() 8
8![]() C
C![]()
![]()
![]() 步骤
步骤![]() 不宜使用NaOH溶液来沉淀
不宜使用NaOH溶液来沉淀![]() 的原因是______。从溶液中得到
的原因是______。从溶液中得到![]() 的实验操作是______、过滤、洗涤、干燥。
的实验操作是______、过滤、洗涤、干燥。
![]() 步骤
步骤![]() 的反应类型是______,步骤
的反应类型是______,步骤![]() 需要隔绝空气的环境,其原因是______。
需要隔绝空气的环境,其原因是______。
![]() 若绿柱石中Be0的含量为
若绿柱石中Be0的含量为![]() ,上述过程生产Be昀产率为
,上述过程生产Be昀产率为![]() ,则1t该绿柱石理论上能生产含镀量
,则1t该绿柱石理论上能生产含镀量![]() 的镀铜台金______t。
的镀铜台金______t。