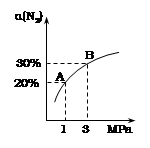题目内容
830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g);△H<0 试回答下列问题:
CO2(g)+H2(g);△H<0 试回答下列问题:
(1)若起始时c(CO)="2" mol?L-1,c(H2O)="3" mol?L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K= .
(2)在相同温度下,若起始时c(CO)="1" mol?L-1,c(H2O)="2" mol?L-1,反应进行一段时间后,测得H2的浓度为0.5 mol?L-1,则此时该反应是否达到平衡状态 (填“是”与“否”), 此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是
。
(3)若降低温度,该反应的K值将 (均填“增大”“减小”或“不变”)。
CO(g)+H2O(g)
 CO2(g)+H2(g);△H<0 试回答下列问题:
CO2(g)+H2(g);△H<0 试回答下列问题:(1)若起始时c(CO)="2" mol?L-1,c(H2O)="3" mol?L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K= .
(2)在相同温度下,若起始时c(CO)="1" mol?L-1,c(H2O)="2" mol?L-1,反应进行一段时间后,测得H2的浓度为0.5 mol?L-1,则此时该反应是否达到平衡状态 (填“是”与“否”), 此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是
。
(3)若降低温度,该反应的K值将 (均填“增大”“减小”或“不变”)。
(1)平衡常数k=1
(2)否 大于 依据是Q=0.5×0.5/0.5×1.5<1即Q<K,所以未达平衡,V(正)>V(逆)
(3)增大
(2)否 大于 依据是Q=0.5×0.5/0.5×1.5<1即Q<K,所以未达平衡,V(正)>V(逆)
(3)增大
试题分析:(1) CO(g)+H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)起始浓度(mol/L) 2 3 0 0
之和浓度(mol/L) 1.2 1.2 1.2 1.2
平衡浓度(mol/L) 0.8 1.8 1.2 1.2
所以平衡常数K=
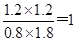
(2)在相同温度下,若起始时c(CO)="1" mol?L-1,c(H2O)="2" mol?L-1,反应进行一段时间后,测得H2的浓度为0.5 mol?L-1,则根据方程式可知,此时CO2的浓度也是0.5mol/L,而CO和水蒸气的浓度分别是0.5mol/L和1.5mol/L,则此时
 <1,所以反应没有达到平衡状态。此时正反应速率大于逆反应速率。
<1,所以反应没有达到平衡状态。此时正反应速率大于逆反应速率。(3)正反应是放热反应,则降低温度,平衡向正反应方向进行,所以该反应的K值将增大。
点评:该题是高考中的常见题型和重要的考点,属于中等难度的试题。试题贴近高考,基础性强,侧重对学生灵活运用基础知识解决实际问题的能力的培养。该题的关键是明确平衡常数的含义、计算依据以及影响因素,如何结合题意灵活运用即可。有利于调动学生的学习兴趣,提高学生的应试能力。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
 zC(g) △H<0。
zC(g) △H<0。 H2(g) + I2(g),达到 平衡状态的标志是
H2(g) + I2(g),达到 平衡状态的标志是  3M + N ;△H<0,其中A.B.M.N均为气态, 在一定条件下达到平衡后, A 在反应混合物中的百分含量为 a% , 若要通过改变条件使 a% 改变为 2a%, 那么下列各项可以改变的条件中应选择的是:
3M + N ;△H<0,其中A.B.M.N均为气态, 在一定条件下达到平衡后, A 在反应混合物中的百分含量为 a% , 若要通过改变条件使 a% 改变为 2a%, 那么下列各项可以改变的条件中应选择的是:  2NH3,下列有关说法正确的是( )
2NH3,下列有关说法正确的是( )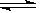 zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是( )
zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是( ) 2C(气)△H < 0,这个可逆反应的正确图像为( )
2C(气)△H < 0,这个可逆反应的正确图像为( )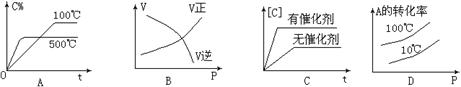
 2NH3(g);△H=-92.2kJ·mol-1。平衡时容器内气体压强为起始时的80%。(写出计算过程)
2NH3(g);△H=-92.2kJ·mol-1。平衡时容器内气体压强为起始时的80%。(写出计算过程) CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol/L,求:(写出计算过程)
CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol/L,求:(写出计算过程)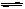 2NH3(g) ;△H=-92.4kJ/mol。
2NH3(g) ;△H=-92.4kJ/mol。