题目内容
1.现有一物质的1H核磁共振谱如图所示:则该物质可能是下列中的( )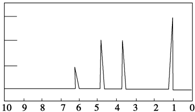
| A. | CH3CH2CH3 | B. | CH3CH2CH2OH | C. | CH3CH2CH2CH3 | D. | CH3CH2CHO |
分析 分子中有几种氢原子核磁共振谱图有几个峰以及等效H的判断方法:
①分子中同一甲基上连接的氢原子等效;
②同一碳原子所连的氢原子等效;
③处于镜面对称位置(相当于平面成像时,物与像的关系)上的氢原子等效.
核磁共振谱有四种峰,说明有四种氢原子.
解答 解:A.CH3CH2CH3有2种不同环境下的氢原子,所以1H核磁共振谱图中有2种峰,故A错误;
B.CH3CH2CH2OH中有4种不同环境下的氢原子,所以1H核磁共振谱图中有4种峰,故B正确;
C.CH3CH2CH2CH3有2种不同环境下的氢原子,所以1H核磁共振谱图中有2种峰,故C错误;
D.CH3CH2CHO有3种不同环境下的氢原子,所以1H核磁共振谱图中有3种峰,故D错误.
故选B.
点评 本题考查核磁共振氢谱,难度不大,根据等效氢判断,注意分子中等效氢的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液,⑥蒸发.正确的操作顺序是( )
| A. | ①④②⑤①③⑥ | B. | ①②⑤④①③⑥ | C. | ①④②⑤③①⑥ | D. | ①②⑤④③①⑥ |
16.下列有关化学用语表示正确的是( )
| A. | 18O2-结构示意图: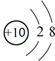 | |
| B. | Na2O2的电子式: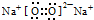 | |
| C. | HCO3- 的水解方程式HCO3-+H2O?H2CO3+OH- | |
| D. | HI的电离方程式 HI?H++I- |
6.A,B,C均为主族元素,其中A原子最外层只有1个电子,B原子的m层上有6个电子,C原子最外层比次外层多4个电子,它们之间可形成化合物M.下列说法中正确的是( )
| A. | M的组成不可能是ABC3或A3BC4 | |
| B. | M的水溶液不可能呈中性 | |
| C. | 用石墨电极电解M的水溶液时,pH不可能减小 | |
| D. | M不可能是离子晶体 |
13.下列离子在溶液中能大量共存的是( )
| A. | Fe3+、NH4+、SCN-、Cl- | B. | Fe2+、H+、NO3-、SO42- | ||
| C. | Fe2+、Fe3+、Na+、NO3- | D. | Fe2+、NH4+、Cl-、OH- |
10.关于石油的说法不正确的是( )
| A. | 石油主要含C H 两种元素 | |
| B. | 石油是主要由各种烷烃 环烷烃和芳香烃所组成的混合物 | |
| C. | 石油有固定的沸点,故可分馏 | |
| D. | 石油分馏得到的汽油是混合物 |
11.下表是部分短周期元素的信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物稳定性:H2T<H2R | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T形成的化合物具有两性 | D. | L2+与R2-具有相同的电子层结构 |
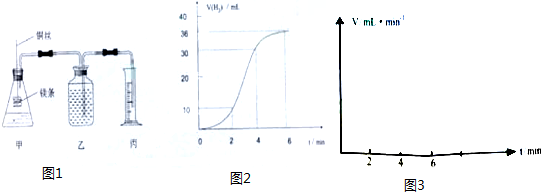
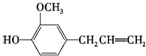 丁子香酚可用作杀虫剂和防腐剂,其结构简式如图:
丁子香酚可用作杀虫剂和防腐剂,其结构简式如图: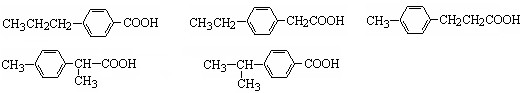 (任意2种)..
(任意2种)..