题目内容
19.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液,⑥蒸发.正确的操作顺序是( )| A. | ①④②⑤①③⑥ | B. | ①②⑤④①③⑥ | C. | ①④②⑤③①⑥ | D. | ①②⑤④③①⑥ |
分析 除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求.
解答 解:泥沙可用过滤除掉,镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,蒸发除掉水和过量的氯化氢,所以正确的顺序为:①过滤,⑤加过量的BaCl2溶液,④加过量的Na2CO3溶液,②加过量的NaOH溶液,①过滤,③加适量的盐酸;或者,②加过量的NaOH溶液,⑤加过量的BaCl2溶液,④加过量的Na2CO3溶液,①过滤,③加适量的盐酸,⑥蒸发.所以正确的顺序是⑤④②①③或②⑤④①③.
故选B.
点评 本题主要考查了除杂质的原则,以及除杂质的顺序,题目难度不大,注意为了将杂质除净,每次所加试剂要过量,这类题时常出现,要加以掌握.

练习册系列答案
相关题目
10.用 NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g铁和足量氯气反应时,铁失去的电子数为0.2 NA | |
| B. | 22.4 L甲烷(CH4)所含的原子数为5 NA | |
| C. | 常温常压下,28 g氮气所含的原子数为2NA | |
| D. | 在20℃,1.01×105Pa时,11.2 L氧气所含的原子数为NA |
7.下列物质间的转化,需要加入氧化剂才能实现的是( )
| A. | Cl2→HClO | B. | Fe2O3→Fe | C. | NH3→NO | D. | H2SO4(浓)→SO2 |
4.有关①100mL 0.1mol/L NaHCO3、②100mL 0.1mol/L Na2CO3两种溶液的叙述不正确的是( )
| A. | 溶液中水电离出的H+个数:②>① | |
| B. | Na2CO3溶液中:c(Na+)=2c(CO32-)+c(H2CO3)+c(HCO3-) | |
| C. | ①溶液中:c(CO${\;}_{3}^{2-}$)<c(H2CO3) | |
| D. | ②溶液中:c(HCO${\;}_{3}^{-}$)>c(H2CO3) |
4.下列提纯方法不正确的是( )
| A. | 除去KNO3中的NaCl杂质----结晶 | |
| B. | 除去食盐中的泥沙-----分液 | |
| C. | 除去KCl中的K2CO3-----加适量硝酸 | |
| D. | 除去碘水中的碘-----萃取 |
1.现有一物质的1H核磁共振谱如图所示:则该物质可能是下列中的( )
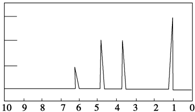

| A. | CH3CH2CH3 | B. | CH3CH2CH2OH | C. | CH3CH2CH2CH3 | D. | CH3CH2CHO |
2.0.4L 1mol/L KCl溶液与0.5L 1mol/L AlCl3溶液中的Cl-的物质的量浓度之比( )
| A. | 15:4 | B. | 3:1 | C. | 4:15 | D. | 1:3 |
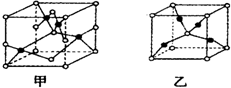 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态.
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态.