题目内容
6.A,B,C均为主族元素,其中A原子最外层只有1个电子,B原子的m层上有6个电子,C原子最外层比次外层多4个电子,它们之间可形成化合物M.下列说法中正确的是( )| A. | M的组成不可能是ABC3或A3BC4 | |
| B. | M的水溶液不可能呈中性 | |
| C. | 用石墨电极电解M的水溶液时,pH不可能减小 | |
| D. | M不可能是离子晶体 |
分析 A、B、C均为主族元素,其中A原子最外层只有1个电子,则A为H、Li、Na、K等ⅠA族元素;B原子的m层上有6个电子,则B为S元素;C原子最外层比次外层多4个电子,原子只能有2个电子层,最外层电子数为6,故C为O元素,三元素可以形成多种化合物M:H2SO4、H2SO3、Na2SO4、Na2SO3、Na2S2O3等,据此解答.
解答 解:A、B、C均为主族元素,其中A原子最外层只有1个电子,则A为H、Li、Na、K等ⅠA族元素;B原子的m层上有6个电子,则B为S元素;C原子最外层比次外层多4个电子,原子只能有2个电子层,最外层电子数为6,故C为O元素,三元素可以形成多种化合物M:H2SO4、H2SO3、Na2SO4、Na2SO3、Na2S2O3等.
A.ABC3、A3BC4中B的化合价均为+5,而S不可能为+5价,故A正确;
B.Na2SO4溶液呈中性,故B错误;
C.电解H2SO4溶液时,实质是电解水,硫酸浓度增大,溶液pH减小,故C错误;
D.Na2SO4、Na2SO3、Na2S2O3均为离子化合物,故D错误,
故选A.
点评 本题考查结构与位置关系应用,注意A元素与化合物M的不确定性,题目具有一定的开放性,是对学生综合能力的考查.

练习册系列答案
相关题目
3.胶体区别于其他分散系的本质特征是( )
| A. | 产生布朗运动 | B. | 产生丁达尔现象 | ||
| C. | 胶体微粒不能穿透半透膜 | D. | 分散质直径在10-7~10-9m之间 |
4.有关①100mL 0.1mol/L NaHCO3、②100mL 0.1mol/L Na2CO3两种溶液的叙述不正确的是( )
| A. | 溶液中水电离出的H+个数:②>① | |
| B. | Na2CO3溶液中:c(Na+)=2c(CO32-)+c(H2CO3)+c(HCO3-) | |
| C. | ①溶液中:c(CO${\;}_{3}^{2-}$)<c(H2CO3) | |
| D. | ②溶液中:c(HCO${\;}_{3}^{-}$)>c(H2CO3) |
14.下列离子在溶液中能大量共存的是( )
| A. | H+、A1O2-、Na+、Cl- | B. | 强碱性溶液:Na+、HCO3-、SO42- | ||
| C. | Fe2+、Fe3+、Na+、NO3- | D. | Fe2+、NH4+、Cl-、OH- |
1.现有一物质的1H核磁共振谱如图所示:则该物质可能是下列中的( )
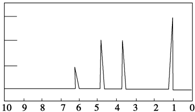

| A. | CH3CH2CH3 | B. | CH3CH2CH2OH | C. | CH3CH2CH2CH3 | D. | CH3CH2CHO |
11.下列叙述正确的是( )
| A. | 无色溶液中:[Ag(NH3)2]+、NH3•H2O、OH-、NO3-可以大量共存 | |
| B. | 常温常压下,22.4L乙烯中含C-H键的数目为4NA(NA表示阿伏加德罗常数的值) | |
| C. | 加入KSCN溶液显红色的溶液中,Na+、Ca2+、HCO3-、Br- 可以大量共存 | |
| D. | 标准状况下,2.24 L NH3溶于1L水中制得氨水,则c(NH3•H2O)=0.1mol•L-1 |
18.Al、Fe、Cu都是重要的金属元素.下列说法正确的是( )
| A. | 三者对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质放置在空气中均只生成氧化物 | |
| C. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 | |
| D. | 冶炼单质Al、Fe、Cu均可采用热还原的方法 |
16.某非金属单质A和氧气恰好完全发生化合反应生成B,B为气体,其体积是氧气体积的两倍(同温同压).以下对B分子组成的推测一定正确的是( )
| A. | 有2个A原子 | B. | 有2个氧原子 | C. | 有1个A原子 | D. | 有1个氧原子 |
 ;
;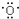 ;
;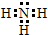 ,结构式为
,结构式为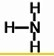 .
.