题目内容
【题目】在密闭容器中,使2 mol A和4 mol B混合发生下列反应:
A(g)+2B(g) ![]() 2C(g) ΔH<0。
2C(g) ΔH<0。
(1)当反应达到平衡时,A和B的浓度比是_______;A和B的转化率比是_______。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_________,密度_________。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度______(填“大于”、“小于”或“等于”)原来的2倍。
【答案】1∶2 1∶1 变小 不变 逆向 向左移动 小于
【解析】
(1)对于A(g)+2B(g) ![]() 2C(g) ΔH<0,在密闭容器中,开始时注入2molA和4molB,发生反应时消耗A和B始终按照1∶2进行,据此分析判断;
2C(g) ΔH<0,在密闭容器中,开始时注入2molA和4molB,发生反应时消耗A和B始终按照1∶2进行,据此分析判断;
(2)根据升高平衡体系的温度时,平衡向逆反应方向移动,根据混合气体的平均相对分子质量![]() =
=![]() ,密度ρ=
,密度ρ=![]() 判断;
判断;
(3)恒压容器中加入惰气,为保持压强不变,容器体积增大,相当于减小压强,据此分析判断;
(4)根据勒夏特列原理解答,若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡向体系温度降低的方向移动,据此分析解答。
(1)对于A(g)+2B(g) ![]() 2C(g) ΔH<0,在密闭容器中,开始时注入2molA和4molB,发生反应时消耗A和B始终按照1∶2进行,所以当反应达到平衡时,剩余A和B的物质的量之比为1∶2,浓度之比也为1∶2;又转化率=
2C(g) ΔH<0,在密闭容器中,开始时注入2molA和4molB,发生反应时消耗A和B始终按照1∶2进行,所以当反应达到平衡时,剩余A和B的物质的量之比为1∶2,浓度之比也为1∶2;又转化率=![]() ,所以A和B的转化率之比为1∶1,故答案为:1∶2;1∶1;
,所以A和B的转化率之比为1∶1,故答案为:1∶2;1∶1;
(2)因为该反应为放热反应,则升高平衡体系的温度时,平衡向逆反应方向移动,气体的物质的量变大,质量不变,所以混合气体的平均相对分子质量![]() =
=![]() 减小,又容器体积不变,所以密度ρ=
减小,又容器体积不变,所以密度ρ=![]() 不变,故答案为:变小;不变;
不变,故答案为:变小;不变;
(3)当达到平衡时,充入氩气,并保持压强不变,体积增大,相当于体系的压强减小,平衡向气体体积增大的方向移动,该反应是气体体积减小的反应,所以平衡逆向移动,故答案为:逆向;
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,该反应为放热反应,升高温度,平衡向吸热的方向移动,即平衡向左移动,使体系温度降低,达到新平衡后,容器内温度小于原来的2倍,故答案为:向左移动;小于。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】将装满气体X的试管倒置于装有液体Y的水槽中,充分振荡试管后,下列说法合理的是
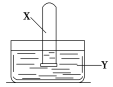
气体X | 液体Y | 试管内现象 | |
A | SO2 | 滴有品红的水溶液 | 无明显现象 |
B | NO2 | 水 | 充满无色溶液 |
C | NH3 | 滴有酚酞的水溶液 | 充满红色溶液 |
D | C2H4 | 酸性KMnO4溶液 | 无明显现象 |
A.AB.BC.CD.D