题目内容
【题目】硼铁混合精矿含有硼镁石[MgBO2(OH)]、磁铁矿(Fe3O4) 、磁黄铁矿(Fe2S)、晶质铀矿(UO2)等,以该矿为原料制备MgSO4H2O和硼酸(H3BO3)的工艺流程如下:
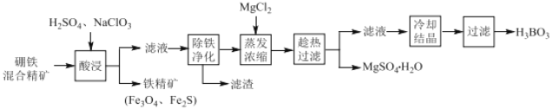
已知:UO22+在pH为4~5的溶液中生成UO2(OH)2沉淀。
回答下列问题:
(1)“酸浸”时,为了提高浸出率可采取的措施有:_______________________(至少答两个措施),该步骤中NaClO3可将UO2转化为UO22+,则该反应的离子方程式为 ________ 。
(2)“除铁净化”需要加入 ______ (填化学式)把溶液pH调节至4~5,滤渣的成分是____。
(3)“蒸发浓缩”时,加入固体MgCl2的作用是 ______________________ 。
(4)铁精矿(Fe3O4、Fe2S)经过一系列加工后,可用于制备氢氧化铁固体。已知T℃Ksp[Fe(OH)3]=4.0×10-39、Ksp[Fe(OH)2]=8.0×10-16 、Kw=10-a,回答下列问题:
①在T℃,假设Fe3+水解的离子方程式是:Fe3+(aq)+3H2O(l)= Fe(OH)3 (s)+3H+(aq),则该条件下Fe3+水解反应的平衡常数K=___________(用含a的字母表示)。
②在T℃向饱和的Fe(OH)3、Fe(OH)2混合溶液中,加入少量NaOH固体(忽略溶液体积变化),则溶液中的![]() 会________(填“变大”“变小”或“不变”),请结合相关数据推理说明:____________________________ 。
会________(填“变大”“变小”或“不变”),请结合相关数据推理说明:____________________________ 。
【答案】将硼铁矿粉碎、适当提高硫酸的浓度、搅拌、升高温度等 3UO2+6H+ +C1O3—= 3UO22-+ +3H2O+C1— MgO Fe(OH)3、UO2(OH)2 增大 Mg2+ 浓度,有利于MgSO4·H2O析出 2.5×10(37—3a) 变大 ![]() =
=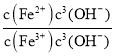 =
=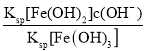 =
=![]() =2.0×1022×c(OH-),加入NaOH固体后,溶液的c(OH—)增大,所以
=2.0×1022×c(OH-),加入NaOH固体后,溶液的c(OH—)增大,所以![]() 变大
变大
【解析】
硼铁混合精矿含有硼镁石[MgBO2(OH)]、磁铁矿(Fe3O4)、磁黄铁矿(Fe2S)、晶质铀矿(UO2)等,加入硫酸、NaClO3,NaClO3可将UO2转化为UO22+,过滤除去少量铁精矿(Fe3O4、Fe2S),调节滤液的pH除铁净化,可生成氢氧化铁、UO2(OH)2沉淀,过滤后的溶液中加入氯化镁,进行蒸发浓缩,趁热过滤可得到硫酸镁晶体,滤液中含有硼酸,冷却结晶得到硼酸(H3BO3)晶体,据此分析解答。
(1)酸浸”时,为了提高浸出率可采取的措施有:搅拌、升高温度、延长浸出时间、适当提高硫酸的浓度,将硼铁矿粉碎等;NaClO3可将UO2转化为UO22+,反应的离子方程式为3UO2+6H++ClO3-=3UO22++3H2O+Cl-,故答案为:将硼铁矿粉碎、适当提高硫酸的浓度、搅拌、升高温度等;3UO2+6H++ClO3-=3UO22++3H2O+Cl-;
(2)除铁净化时,调节pH,需要避免引入新杂质,可加入MgO或Mg(OH)2等,生成的沉淀为Fe(OH)3、UO2(OH)2,故答案为:MgO或Mg(OH)2;Fe(OH)3、UO2(OH)2;
(3)“蒸发浓缩”时,加入固体MgCl2,可使溶液中镁离子浓度增大,有利于析出MgSO4H2O,故答案为:增大镁离子浓度,有利于析出MgSO4H2O;
(4)①在T℃,Fe3+水解方程式为Fe3+(aq)+3H2O(l)═Fe(OH)3(s)+3H+(aq),则该条件下Fe3+水解反应的平衡常数K=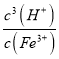 =
=![]() =
=![]() =2.5×10(37-3a),故答案为:2.5×10(37-3a);
=2.5×10(37-3a),故答案为:2.5×10(37-3a);
②![]() =
=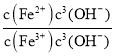 =
=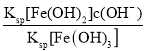 =
=![]() =2.0×1022×c(OH-),在T℃向饱和Fe(OH)3、Fe(OH)2的混合溶液中,加入少量NaOH固体,溶液中的c(OH-)增大,则
=2.0×1022×c(OH-),在T℃向饱和Fe(OH)3、Fe(OH)2的混合溶液中,加入少量NaOH固体,溶液中的c(OH-)增大,则![]() 变大,故答案为:变大;
变大,故答案为:变大;![]() =
=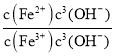 =
=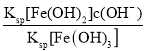 =
=![]() =2.0×1022×c(OH-),加入少量NaOH固体,溶液中的c(OH-)增大,则
=2.0×1022×c(OH-),加入少量NaOH固体,溶液中的c(OH-)增大,则![]() 变大。
变大。