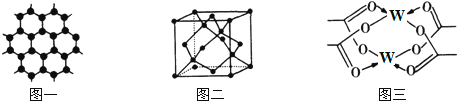
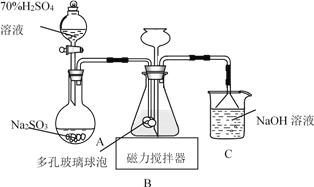
题目内容
【题目】X、Y、Z、Q为短周期非金属元素,R是长周期元素。X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+只有三个电子层且完全充满电子。请回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)R的基态原子的电子排布式为 。
(2)X、Y、Z三种元素第一电离能从大到小顺序为 。
(3)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键):
![]()
①该分子中两个Y原子之间的键型组合正确的是 。
A.仅1个σ键
B.1个σ键和2个π键
C.1个σ键和1个π键
D.仅2个σ键
②该分子中Y原子的杂化方式是 。
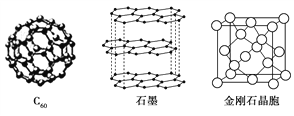
(4)X与Y元素可以形成一种超硬新材料,其晶体部分结构如下图所示,有关该晶体的说法正确的是 。

A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时共价键被破坏,没有克服范德华力和氢键
【答案】(1)1s22s22p63s23p63d104s1(或[Ar]3d104s1)
(2)N>O>C (3)①C ②sp2 (4)B、C、D
【解析】由题意可知X为碳元素,Y为氮元素,Z为氧元素,Q为氟元素,R为铜元素。
(1)Cu为29号元素,电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。
(2)C、N、O三种元素的第一电离能由大到小的顺序为N>O>C。
(3)由N2F2的两种结构可知,其结构式为
 和
和![]()
两个N原子以双键形式成键,存在1个σ键和1个π键,C项正确;N原子采取sp2杂化。
(4)观察图形可发现与C原子相连的有4个N原子,与N原子相连的有3个C原子,形成了空间立体网状结构。可知该晶体为原子晶体,化学式为C3N4,晶体熔化时,化学键被破坏,故A项错误,C、D两项正确。对原子晶体而言,键长越短,其硬度越大,由于C—C键的键长大于C—N键的键长,故该晶体的硬度比金刚石还大,B项正确。

 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案