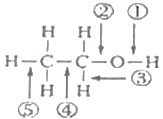
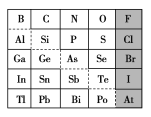
籾朕坪否
‐籾朕/↙1⇄械梁和⇧壓200 mL狽剳晒欝卑匣嶄根嗤1〜10-3mol議欝宣徨⇧繍緩卑匣嚥pH﹆3議冦磨詞栽⇧聞凪詞栽卑匣議pH﹆7⇧哘函狽剳晒欝卑匣才冦磨議悶持岻曳頁_________。
↙2⇄25≧扮⇧旋喘pH編崕霞誼0.1molL-1閑磨卑匣議pH埃葎3⇧夸辛參浩麻竃閑磨議窮宣械方埃葎_______◉﨑10mL緩卑匣嶄紗秘富楚甥閑磨⇧策待卑盾狛殻嶄卑匣梁業才悶持議裏弌延晒⇧卑匣嶄c↙H⇦⇄/c↙CH3COOH⇄議峙繍_____↙野^奐寄 ̄、^受弌 ̄賜^涙隈鳩協 ̄⇄。
↙3⇄窮晒僥隈頁栽撹葦議匯嶽仟圭隈⇧凪圻尖泌夕侭幣⇧咐自議窮自郡哘塀頁_____。

↙4⇄系邦嶄根紀晒栽麗議侃尖圭隈嗤謹嶽。
〙 NaClO卑匣辛繍系邦嶄議NH4+廬晒葎N2。飛侃尖狛殻嶄恢伏N2 0.672 L↙炎彈彜趨⇄⇧夸俶勣嶧債0.3 mol,L-1議NaClO卑匣______________L。
〖壓裏伏麗議恬喘和⇧NH4+将狛曾化郡哘氏廬晒葎NO3-⇧曾化郡哘議嬬楚延晒泌夕侭幣。夸1 mol NH4+(aq)畠何瓜剳晒撹NO3-(aq)扮慧竃議犯楚頁______________kJ。
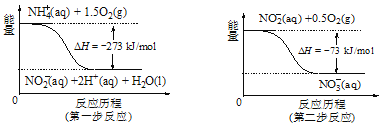
〗 喘H2岸晒珊圻隈辛週詰邦嶄NO3-議敵業⇧誼欺議恢麗嬬歌嚥寄賑儉桟⇧夸郡哘朔卑匣議pH______↙野^幅互 ̄、^週詰 ̄賜^音延 ̄⇄。
↙5⇄械梁和⇧喘NaOH卑匣恬CO2俺彌質音叙辛參週詰娘電慧⇧遇拝辛誼欺嶷勣議晒垢恢瞳Na2CO3。飛蝶肝俺彌朔誼欺pH=10 議卑匣⇧夸卑匣c(CO32-)|c(HCO3-)=_______。 [械梁和K1(H2CO3)=4.4〜10-7、 K2(H2CO3)=5〜10-11]。
‐基宛/1⦿1010-5mol,L⇩1受弌N2+6H++6e- = 2NH30.3346幅互1⦿2賜0.5
‐盾裂/
↙1⇄壓Ba(OH)2卑匣嶄⇧Ba2+才OH-議麗嵎議楚岻曳葎1⦿2⇧絞n↙OH-⇄=2n↙Ba2+⇄=2〜10-3mol◉pH﹆3議冦磨嶄c↙H+⇄=10-3mol/L⇧譜冦磨卑匣議悶持葎V⇧功象詞栽朔卑匣𠮟嶄來⇧夸n↙OH-⇄=n↙H+⇄⇧軸2〜10-3mol =10-3mol/L〜V⇧盾誼V=2L=2000mL⇧絞哘函狽剳晒欝卑匣才冦磨議悶持岻曳頁200mL:2000mL=1:10◉
↙2⇄25≧扮⇧旋喘pH編崕霞誼0.1molL-1閑磨卑匣議pH埃葎3⇧樋窮盾嵎贋壓窮宣峠財⇧CH3COOHCH3COO-+H+⇧械方Ka=![]() ⇧閑磨卑匣議pH埃葎3⇧狽宣徨才閑磨功宣徨敵業葎10-3mol/L⇧卑匣嶄閑磨卑嵎敵業除貌葎0.1mol/L⇧夸辛參浩麻竃閑磨議窮宣械方埃葎
⇧閑磨卑匣議pH埃葎3⇧狽宣徨才閑磨功宣徨敵業葎10-3mol/L⇧卑匣嶄閑磨卑嵎敵業除貌葎0.1mol/L⇧夸辛參浩麻竃閑磨議窮宣械方埃葎![]() =10-5mol/L⇧﨑10mL緩卑匣嶄紗秘富楚甥閑磨⇧卑盾朔閑磨卑匣敵業奐寄⇧閑磨窮宣殻業受弌⇧
=10-5mol/L⇧﨑10mL緩卑匣嶄紗秘富楚甥閑磨⇧卑盾朔閑磨卑匣敵業奐寄⇧閑磨窮宣殻業受弌⇧![]() 曳峙受弌◉
曳峙受弌◉
(3) 功象狽宣徨卞強圭﨑辛岑⇧宥秘狽賑極葎剩自⇧宥秘紀賑極葎咐自⇧咐自貧紀賑誼欺窮徨伏撹葦賑⇧窮自郡哘塀葎N2+6H++6e- = 2NH3◉
↙4⇄〙N払肇窮徨⇧Cl誼欺窮徨⇧譜嶧債0.3molL-1議NaClO卑匣葎xL⇧喇窮徨便冴辛岑⇧0.3mol〜xL〜2=![]() 〜2〜3⇧盾誼x=0.3◉
〜2〜3⇧盾誼x=0.3◉
〖喇夕辛岑⇧及匯化犯晒僥郡哘葎NH4+ ↙aq⇄+1.5O2↙g⇄=2H+↙aq⇄+NO2- ↙aq⇄+H2O↙l⇄@H=-273 kJmol-1〙⇧及屈化犯晒僥郡哘葎NO2- ↙aq⇄+0.5O2↙g⇄=NO3- ↙aq⇄@H=-73kJmol-1〖⇧喇固帽協舵辛岑〙+〖誼1mol NH4+↙aq⇄畠何剳晒撹NO3- ↙aq⇄議犯晒僥圭殻塀葎NH4+ ↙aq⇄+2O2↙g⇄=2H+↙aq⇄+NO3- ↙aq⇄+H2O↙l⇄@H=-346 kJmol-1⇧軸慧竃346kJ議犯楚◉
〗H2岸晒珊圻咬喘邦嶄NO3-⇧郡哘嶄議珊圻恢麗才剳晒恢麗譲辛歌嚥寄賑儉桟⇧夸恢麗葎邦才紀賑⇧乎郡哘葎5H2+2NO3-![]() N2+4H2O+2OH-⇧狽剳功宣徨敵業奐寄⇧夸pH幅互◉
N2+4H2O+2OH-⇧狽剳功宣徨敵業奐寄⇧夸pH幅互◉
↙5⇄飛蝶肝俺彌朔誼欺pH=10 議卑匣⇧夸卑匣磨珠來麼勣畳協CO32-+ H2O ![]() HCO3-+ OH-⇧K=
HCO3-+ OH-⇧K=![]() ⇧c(CO32-)|c(HCO3-)=
⇧c(CO32-)|c(HCO3-)=![]() 。
。

 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛