题目内容
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
NaCl溶于水 |
电解CuCl2溶液 |
CH3COOH在水中电离 |
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D
【答案】B
【解析】
本题A、B、C选项应区分电离和电解的概念。电离是电解质溶于水或熔融状态下,解离成能够自由移动的离子的过程。根据其电离程度可分为强电解质和弱电解质,几乎全部电离的是强电解质(如A选项),只有少部分电离的是弱电解质(如C选项);是将电能转化为化学能的一个装置(构成:外加电源,电解质溶液,阴阳电极)。使电流通过电解质溶液或熔融电解质而在阴,阳两极引起还原氧化反应的过程(如B选项)。
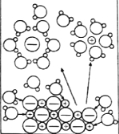
A.NaCl为强电解质,NaCl溶于水,NaCl在水分子作用下,自发解离为Na+和Cl-,故电离方程式为NaCl=Na++Cl-,故A不符合题意;
B.电解氯化铜溶液,铜离子向阴极移动,得电子,发生电极反应为:Cu2++2e-=Cu,氯离子向阳极移动,失电子,发生电极反应为:2Cl-+2e-=Cl2,所以电解总反应为:Cu2++2Cl-![]() Cu+Cl2,故B符合题意;
Cu+Cl2,故B符合题意;
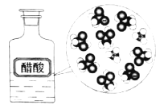
C.CH3COOH为弱电解质,溶于水部分电离,因此电离方程式为CH3COOH![]() CH3COO-+H+,故C不符合题意;
CH3COO-+H+,故C不符合题意;
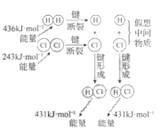
D.由图可知,反应H2(g)+Cl2(g)=2HCl(g)的反应热等于断裂反应物分子中的化学键吸收的总能量(436kJ/mol+243kJ/mol=679kJ/mol),与形成生成物分子中化学键放出的总能量(431kJ/mol×2=862kJ/mol)之差,即放热183kJ/mol,放热H为负值,所以H2(g)+Cl2(g)=2HCl(g)H=-183kJ/mol,故D不符合题意;
综上所述,本题应选B。