题目内容
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见
| A.复分解反应都是吸热反应 |
| B.NH4HCO3和盐酸的反应是吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.反应的热化学方程式为:NH4HCO3+HCl=NH4Cl+CO2↑+H2O△H>0 |
B
解析试题分析:解:如氯化铵与氢氧化钡的反应是吸热反应,但酸碱中和反应是放热反应,故A错误;B、因反应为吸热反应,即吸热的热量转化为产物内部的能量,故B正确;C、因反应为吸热反应,则反应后生成物的总能量高于反应物的总能量,故C错误;D、书写热化学方程式时,应注明物质的状态,故D错误;故选B.
考点:本题考查化学反应能量变化判断,热化学方程式书写方法,能量守恒的应用分析是解题关键,题目难度中等。

下列说法正确的是
| A.天然气、石油都是清洁的可再生能源 |
| B.在燃煤中添加碳酸钙或生石灰可以减少SO2的排放 |
| C.在AgC1饱和溶液中加入AgNO3溶液,达平衡时,溶液中Ksp(AgCl)降低 |
| D.地沟油和矿物油都属于酯类物质 |
反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为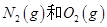 反应生成
反应生成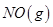 过程中的能量变化,下列说法正确的是
过程中的能量变化,下列说法正确的是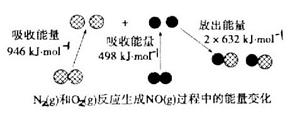
A.通常情况下,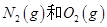 混合能直接生成NO 混合能直接生成NO |
B.1mol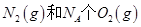 反应放出的能量为180kJ 反应放出的能量为180kJ |
| C.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
D.1mol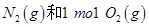 具有的总能量小于2mol 具有的总能量小于2mol 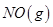 具有的总能量 具有的总能量 |
根据碘与氢气反应的热化学方程式
(1)I2(g)+ H2(g) 2HI(g) ΔH=-9.48 kJ/mol
2HI(g) ΔH=-9.48 kJ/mol
(2)I2(s)+ H2(g) 2HI(g) ΔH=+26.48 kJ/mol
2HI(g) ΔH=+26.48 kJ/mol
下列判断正确的是
| A.254 g I2(g)中通入2 gH2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(2)的反应物总能量比反应(1)的反应物总能量低 |
| D.反应(1)的产物比反应(2)的产物稳定 |
下列说法中正确的是
| A.同温同压下,H2(g)+Cl2(g)= 2HCl(g)在光照条件下和点燃条件下的ΔH不同 |
| B.常温下,2A(s)+B(g)= 2C(g)+D(g)不能自发进行,则该反应焓变一定大于零 |
| C.1mol硫酸与1molBa(OH)2完全中和所放出的热量为中和热 |
| D.在25℃、101KPa时,2mol S的燃烧热是1mol S的2倍 |
下列反应中的能量变化关系符合下图所示的是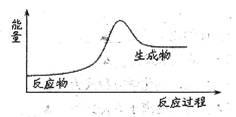
| A.盐酸与烧碱反应 | B.天然气燃烧 |
| C.三氧化硫与水反应 | D.煅烧石灰石 |
H2和I2在一定条件下能发生反应:H2(g) +I2(g) 2HI(g) △H=—a kJ·mol-1
2HI(g) △H=—a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是
| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 |
| C.断开2 mol H-I键所需能量约为(c+b+a) kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
已知1 mol红磷转化为1 mol白磷,吸收18.39 kJ热量。
①4P(红,s)+5O2(g)=2P2O5(s);ΔH1
②P4(白,s)+5O2(g)=2P2O5(s);ΔH2
则ΔH1与ΔH2的关系正确的是( )
| A.ΔH1=ΔH2 | B.ΔH1>ΔH2 |
| C.ΔH1<ΔH2 | D.无法确定 |
在100 g炭不完全燃烧所得气体中CO和CO2的体积比为1∶2。已知:
C(s)+1/2O2(g)=CO(g) ΔH1=-110.35 kJ/mol
CO(g)+1/2O2 =CO2(g) ΔH2=-282.57 kJ/mol
则与100 g炭完全燃烧相比,损失的热量是( )
| A.392.93 Kj | B.2 489.42 kJ |
| C.784.92 kJ | D.3 274.3 kJ |