��Ŀ����
����Ŀ���������ȣ�ClO2)�����Ϲ�����������֯��WHO)��ΪA��Ч��ȫ����������������¶�������Ϊ����ɫ���壬���۵�Ϊ-59.5�棬�е�Ϊ11.0�棬������ˮ������ˮ��Ӧ���¶ȹ��ߣ��������ȵ�ˮ��Һ���ܱ�ը��ij�о���ѧϰС��������ͼ��ʾװ����ȡ���ռ�ClO2�������Ⱥͼг�װ�þ�ʡ�ԣ�

(1)��Բ����ƿ���ȷ���һ������KClO3�Ͳ���(H2C2O4)��Ȼ���ټ���������ϡ���ᣬ��60�桫80��֮������C1O2��CO2��һ�������Σ��÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
(2)Aװ����ʹ���¶ȼƵ�Ŀ��________________����Ӧ��ʼ���Թ۲쵽Բ����ƿ�ڵ�������________��
(3)Bװ�õ�������______________��
(4)Dװ���е�NaOH��Һ����β���е�ClO2���������ʵ���֮��Ϊ��1��1�������Σ�һ��ΪNaClO2����һ��Ϊ________��
(5)ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1����ȡClO2��Һ10.0mL��ϡ�ͳ�100.,0mL��������ȡV1mL�������뵽��ƿ�У�
����2������������pH��2.0������������KI���壬����Ƭ�̣�
����3������ָʾ��X����cmol��L-1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2mL��
(��֪��2ClO2+8H++10I-=5I2+2Cl-+4H2O��2Na2S2O3+I2=Na2S4O6+2NaI)
ָʾ��XΪ________��ԭClO2��Һ��Ũ��Ϊ_________g��L-1(�ú���ĸ�Ĵ���ʽ��ʾ)��
(6)��ͬѧ��ΪKC1O3����������������ᷴӦ������KCl�������ʵ��֤��Aװ�÷�Ӧ�����Һ���Ƿ����C1-����Ҫд�������Լ���ʵ�����������ͽ��ۡ�����֪��AgClO3������ˮ��
_____________________________��
���𰸡� 2KClO3��H2C2O4��H2SO4![]() K2SO4��2ClO2����2H2O��2CO2�� �����¶ȣ������¶ȹ�������ը ��Һ���������ݳ���Բ����ƿ�ڲ�������ɫ���� ��C1O2�������ռ� NaClO3 ������Һ
K2SO4��2ClO2����2H2O��2CO2�� �����¶ȣ������¶ȹ�������ը ��Һ���������ݳ���Բ����ƿ�ڲ�������ɫ���� ��C1O2�������ռ� NaClO3 ������Һ ![]() ȡ����Aװ�÷�Ӧ�����Һ���Թ��У���������Ba(NO3)2��Һ����ַ�Ӧ���ã�ȡ�ϲ���Һ���Թ��У����������ữ����������Һ���۲��Ƿ��а�ɫ�������������У������Cl-�����ޣ�����Cl-
ȡ����Aװ�÷�Ӧ�����Һ���Թ��У���������Ba(NO3)2��Һ����ַ�Ӧ���ã�ȡ�ϲ���Һ���Թ��У����������ữ����������Һ���۲��Ƿ��а�ɫ�������������У������Cl-�����ޣ�����Cl-
�����������⿼��ʵ�鷽����������ۣ���1�����������Ϣ����������K2SO4��KClO3�Ͳ���(H2C2O4)��Ȼ���ټ���������ϡ���ᣬ��60�桫80��֮������ClO2��CO2��һ�������Σ������KClO3��H2C2O4��H2SO4��ClO2����CO2����K2SO4��H2O��KClO3��Cl�Ļ��ϼ��ɣ�5�ۡ���4�ۣ����ϼ۽���1�ۣ�H2C2O4��C�ɣ�3�ۡ���4�ۣ����ϼ۹�����2�ۣ���С��������2��Ȼ�����ԭ���غ㣬��ƽ��������2KClO3��H2C2O4��H2SO4 ![]() K2SO4��2ClO2����2H2O��2CO2������2���¶ȹ��ߣ��������ȵ�ˮ��Һ���ܱ�ը���Լ�60�桫80��֮������ClO2������¶ȼƵ������ǿ����¶ȣ���ֹ�¶ȹ�������ը��ClO2�ǻ���ɫ���壬��˷�Ӧ��ʼ����ƿ�ڵ���������Һ���������ݳ���Բ����ƿ�ڲ�������ɫ���壻��3��ClO2�۵�Ϊ-59.5�棬�е�Ϊ11.0�棬���װ��B�������ǽ�ClO2�������ռ�����4��ClO2��Cl�ԣ�4�ۣ�NaClO2�е�Cl�Ļ��ϼ�Ϊ��3�ۣ��˷�Ӧ��������ԭ��Ӧ���л��ϼ۵����߾��л��ϼ۽��ͣ�����һ��������Ԫ�صĻ��ϼ�ΪX�����������ε����ʵ���Ϊ1��1�����ݵ�ʧ������Ŀ�غ㣬1��1=1��(X��4)����X=5������ΪNaClO3����5����Ϊ������ⵥ�ʱ��������ѡ�õ�ָʾ��Ϊ������Һ������������Ӧ����ʽ�������Ĺ�ϵ��2ClO2��5I2��10Na2S2O3�����ClO2��Ũ��Ϊ��
K2SO4��2ClO2����2H2O��2CO2������2���¶ȹ��ߣ��������ȵ�ˮ��Һ���ܱ�ը���Լ�60�桫80��֮������ClO2������¶ȼƵ������ǿ����¶ȣ���ֹ�¶ȹ�������ը��ClO2�ǻ���ɫ���壬��˷�Ӧ��ʼ����ƿ�ڵ���������Һ���������ݳ���Բ����ƿ�ڲ�������ɫ���壻��3��ClO2�۵�Ϊ-59.5�棬�е�Ϊ11.0�棬���װ��B�������ǽ�ClO2�������ռ�����4��ClO2��Cl�ԣ�4�ۣ�NaClO2�е�Cl�Ļ��ϼ�Ϊ��3�ۣ��˷�Ӧ��������ԭ��Ӧ���л��ϼ۵����߾��л��ϼ۽��ͣ�����һ��������Ԫ�صĻ��ϼ�ΪX�����������ε����ʵ���Ϊ1��1�����ݵ�ʧ������Ŀ�غ㣬1��1=1��(X��4)����X=5������ΪNaClO3����5����Ϊ������ⵥ�ʱ��������ѡ�õ�ָʾ��Ϊ������Һ������������Ӧ����ʽ�������Ĺ�ϵ��2ClO2��5I2��10Na2S2O3�����ClO2��Ũ��Ϊ�� 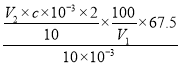 g��L��1=
g��L��1=![]() g��L��1����6����ΪKClO3����ᷴӦ�����������ԣ�����Ϊ���ᣬ��˼���Cl��ʱ��Ӧ�ȳ�ȥSO42��������������ǣ�ȡ����Aװ�÷�Ӧ�����Һ���Թ��У���������Ba(NO3)2��Һ����ַ�Ӧ���ã�ȡ�ϲ���Һ���Թ��У����������ữ����������Һ���۲��Ƿ��а�ɫ�������������У������Cl�������ޣ�����Cl����
g��L��1����6����ΪKClO3����ᷴӦ�����������ԣ�����Ϊ���ᣬ��˼���Cl��ʱ��Ӧ�ȳ�ȥSO42��������������ǣ�ȡ����Aװ�÷�Ӧ�����Һ���Թ��У���������Ba(NO3)2��Һ����ַ�Ӧ���ã�ȡ�ϲ���Һ���Թ��У����������ữ����������Һ���۲��Ƿ��а�ɫ�������������У������Cl�������ޣ�����Cl����

 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�



