题目内容
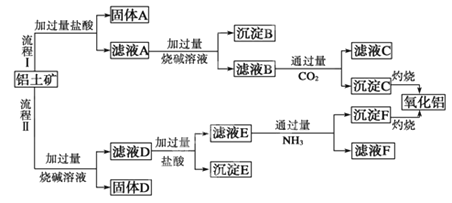
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种流程如下:
请回答下列问题:
(1)给滤液E中通入过量的NH3,其反应的离子方程式是____________________。
(2)流程Ⅱ中加入烧碱溶液后,生成SiO![]() 的离子方程式是__________________。
的离子方程式是__________________。
(3)验证滤液A中含Fe3+,可取少量滤液并加入______________(填写试剂名称)。
(4)滤液C中溶质的主要成分是___________(填化学式)。
(5)滤液F中离子电荷守恒的关系式为___________________________。
(6)滤液C和滤液F共同的溶质为G,用惰性电极电解500mL 0.1 mol·L-1的G溶液,若阳极得56 mL气体(标准状况),则所得溶液在常温下pH为_____________(忽略电解前后溶液体积的变化)。
(7)已知25 ℃时Mg(OH)2的溶度积常数Ksp=1.8×10-11。取适量的滤液A,加入一定量的烧碱溶液至达到沉淀溶解平衡,测得该溶液的pH=13.00,则25℃时残留在溶液中的c(Mg2+)=________ mol·L-1。
【答案】Al2O3+6H+===2Al3++3H2O,Al3++3NH3·H2O===Al(OH)3↓+3NH4+ SiO2+2OH-===SiO32-+H2O 硫氰化钾(或硫氰酸钾、苯酚溶液等合理答案) NaCl、NaHCO3 c(NH4+)+ c(Na+)+ c(H+)= c(OH-)+ c(Cl-) 12 1.8×10-9
【解析】
Al2O3、SiO2、Fe2O3、MgO中,Al2O3、SiO2与NaOH溶液反应,生成NaAlO2和Na2SiO3在D溶液中,过滤残渣D是不与NaOH溶液反应的MgO、Fe2O3;NaAlO2和Na2SiO3的溶液,加入盐酸,溶液E中有AlCl3、NaCl和HCl溶质,滤去的固体E是H2SiO3;溶液E中通入NH3,固体F是Al(OH)3,灼烧后为氧化铝,溶液F含NaCl和NH4Cl。
铝土矿中除SiO2不与盐酸反应外,Al2O3、Fe2O3、MgO均与盐酸反应,故A溶液中有AlCl3、FeCl3、MgCl2和HCl;在加入过量烧碱,生成沉淀B是Fe(OH)3和Mg(OH)2,溶液B中有NaAlO2和NaOH;溶液B中通入过量CO2,溶液C是NaCl和NaHCO3两种溶质,产生C沉淀是Al(OH)3;Al(OH)3灼烧生成Al2O3,据以上分析解答。
Al2O3、SiO2、Fe2O3、MgO中,Al2O3、SiO2与NaOH溶液反应,生成NaAlO2和Na2SiO3在D溶液中,过滤残渣D是不与NaOH溶液反应的MgO、Fe2O3;NaAlO2和Na2SiO3的溶液,加入盐酸,溶液E中有AlCl3、NaCl和HCl溶质,滤去的固体E是H2SiO3;溶液E中通入NH3,固体F是Al(OH)3,溶液F含NaCl和NH4Cl;
铝土矿中除SiO2不与盐酸反应外,Al2O3、Fe2O3、MgO均与盐酸反应,故A溶液中有AlCl3、FeCl3、MgCl2和HCl;在加入过量烧碱,生成沉淀B是Fe(OH)3和Mg(OH)2,溶液B中有NaAlO2和NaOH;溶液B中通入过量CO2,溶液C是NaCl和NaHCO3两种溶质,产生C沉淀是Al(OH)3;Al(OH)3灼烧生成Al2O3;
(1)给滤液E中通入过量的NH3,其反应的离子方程式是Al2O3+6H+===2Al3++3H2O,Al3++3NH3·H2O===Al(OH)3↓+3NH4+;
(2)流程Ⅱ中加入烧碱溶液后,生成SiO![]() 的离子方程式是SiO2+2OH-===SiO32-+H2O;
的离子方程式是SiO2+2OH-===SiO32-+H2O;
(3)验证滤液A中含Fe3+,可取少量滤液并加入硫氰化钾或硫氰酸钾或苯酚溶液等;
(4)滤液C中溶质的主要成分是NaCl、NaHCO3;
(5)滤液F(NaCl和NH4Cl)中离子电荷守恒的关系式为c(NH4+)+ c(Na+)+ c(H+)= c(OH-)+ c(Cl-);
(6)滤液C和滤液F共同的溶质为NaCl,用惰性电极电解500mL 0.1 mol·L-1的NaCl溶液,阳极得56 mL气体Cl2(标准状况);2NaCl+2H2O![]() H2↑+Cl2↑+2NaOH,n(NaOH)=2n(Cl2)=
H2↑+Cl2↑+2NaOH,n(NaOH)=2n(Cl2)= ![]() =0.005mol,溶液中故c(NaOH)=0.01mol/L,pOH=2,pH=12;
=0.005mol,溶液中故c(NaOH)=0.01mol/L,pOH=2,pH=12;
(7) pH=13.00时,c(OH-)=0.1 mol·L-1,Ksp=c(Mg2+)·c2(OH-)=1.8×10-11,可得c(Mg2+)=1.8×10-9mol·L-1。

【题目】关于下列各图的叙述不正确的是( )
化学方程式 | 平衡常数K |
F2 + H2 = 2HF | 6.5×1095 |
Cl2 + H2 = 2HCl | 2.6×1033 |
Br2 + H2 = 2HBr | 1.9×1019 |
I2 + H2 = 2HI | 8.7×102 |
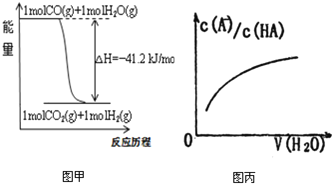
A.已知CO的燃烧热283kJ·mol-1,O2(g) +2 H2(g) = 2H2O(g) ΔH = -483.6 kJ·mol-1,则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.某温度下,pH =11的NH3H2O和pH =1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3H2O与NH3三种微粒的平衡浓度之和为0.05molL-1
C.在常温下,X2(g) 和 H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,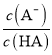 的变化情况
的变化情况