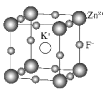
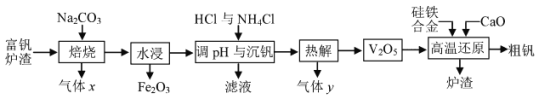
��Ŀ����
����Ŀ��Cu��������������������������Ҫ��Ӧ�á�
I.����Cu2O���Ǻ�ĸ��ͧ�ײ��ķ���ʴͿ�ϣ�Ҳ�������Ĵ�����
��1����֪��Cu2O(s)+![]() O2(g)=2CuO(s) ��H=-196kJ/mol
O2(g)=2CuO(s) ��H=-196kJ/mol
2C(s)+O2(g)=2CO(g) ��H=-220.8kJ/mol
��ҵ����̼����CuO��ĩ�����һ�������·�Ӧ��ȡCu2O(s)��ͬʱ����CO������Ȼ�ѧ����ʽΪ___��
��2��������Cu2O��������ʵ�ּ״�������ȡ��ȩ��CH3OH(g)![]() HCHO(g)+H2(g)���״���ƽ��ת�������¶ȱ仯������ͼ��ʾ��
HCHO(g)+H2(g)���״���ƽ��ת�������¶ȱ仯������ͼ��ʾ��
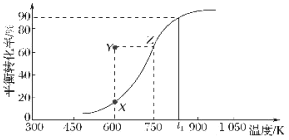
�ٸ÷�Ӧ����H___0������>������<������600Kʱ��Y��״���v������___v���棩������>������<������
����t1Kʱ����̶����Ϊ1L���ܱ������г���2molCH3OH(g)���¶ȱ��ֲ��䣬9����ʱ�ﵽƽ�⣬��0��9min����CH3OH(g)��ʾ�ķ�Ӧ����v(CH3OH)___���¶�Ϊt1ʱ���÷�Ӧ��ƽ�ⳣ��K��ֵΪ___��
II.Cu���dz����Ĵ��������dz����ĵ缫���ϡ�
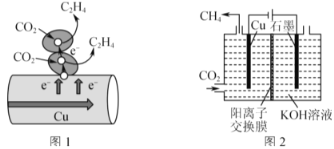
��3��ͼ1��ʾ��������CO2����ֱ�ӵ��Ӵ��ݻ��������ڴ���ͭ�ı������ת������ֱ�Ӵ��ݵĵ������ʵ���Ϊ2molʱ����μӷ�Ӧ��CO2�����ʵ���Ϊ___��
��4��ͼ2��ʾ��KOH��Һ���������Һ���е���ʾ��ͼ��CO2��Cu�缫�Ͽ���ת��ΪCH4���õ缫��Ӧ�ķ���ʽΪ___��
III.��ͭ���ӵķ�ˮ�������Ⱦ��ͨ������ת��Ϊ��ͭ��������ȥ��
��5����֪��Ksp(CuS)=1��10-36��Ҫʹͭ���ӵ�Ũ�ȷ����ŷű���������0.4mg/L������Һ�е������ӵ����ʵ���Ũ������Ϊ___mol/L��������С�����һλ����
���𰸡�C(s)+ 2CuO(s)= Cu2O(s)+ CO(g) ��H=+85.6 kJ/mol �� �� 0.2mol��L-1��min-1 16.2 0.33mol CO2+8e-+6H2O=CH4+8OH- ![]()
��������
��2���������������ļ״�ת�������¶ȱ仯����ͼ�����Կ��������¶����ߣ��״���ת�������������¶���ת���ʵĹ�ϵ�������жϳ���Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ�����������ϵĵ㶼��ƽ��״̬��Y��ʱ��ת���ʸ���X�㣬����ͬ�¶��£�Ҫ�ﵽƽ�⣬�������淴Ӧ�ķ�Ӧ���������ж�Y������淴Ӧ���ʵĴ�С��
��5��һ����Ϊ��Һ��ij����Ũ��С��10-5mol/L������Ϊ�������ѳ�����ȫ�����ݸ����ۣ�������о�����ֵ�����м��㡣ע�����е�λ��ת����
I.��1��������֪������Cu2O(s)+![]() O2(g)=2CuO(s) ��H=-196kJ/mol ��
O2(g)=2CuO(s) ��H=-196kJ/mol ��
2C(s)+O2(g)=2CO(g) ��H=-220.8kJ/mol ��
����Ŀ���Ȼ�ѧ����ʽ����֪��![]() �ɵ�Ŀ���Ȼ�ѧ����ʽ��C(s)+ 2CuO(s)= Cu2O(s)+ CO(g) ��H=
�ɵ�Ŀ���Ȼ�ѧ����ʽ��C(s)+ 2CuO(s)= Cu2O(s)+ CO(g) ��H=![]() ����Ϊ��C(s)+ 2CuO(s)= Cu2O(s)+ CO(g) ��H=+85.6 kJ/mol��
������C(s)+ 2CuO(s)= Cu2O(s)+ CO(g) ��H=+85.6 kJ/mol��
��2�������������Ϣ�����Կ��������¶ȵ����״���ƽ��ת����������˵���÷�Ӧ������ӦΪ���ȷ�Ӧ����H��0��600Kʱ��Y��ת���ʴ���X���ƽ��ת���ʣ�Y��X�㣬�״���ת���ʽ��ͣ�˵����Ӧ���淴Ӧ������У���v��������v���棩����Ϊ����������
����ͼ��֪����t1Kʱ���״���ƽ��ת����Ϊ90%����̶����Ϊ1L���ܱ������г���2molCH3OH(g)���¶ȱ��ֲ��䣬9����ʱ�ﵽƽ�⣬ƽ��ʱ���״������ʵ���Ϊ0.2mol����ȩ�����ʵ���Ϊ1.8mol��H2�����ʵ���Ϊ1.8mol����ƽ��ʱ�״������ʵ���Ũ��Ϊ0.2mol/L����ȩ�����ʵ���Ũ��Ϊ1.8 mol/L��H2�����ʵ���Ũ��Ϊ1.8mol/L��0��9min����CH3OH(g)��ʾ�ķ�Ӧ����v(CH3OH)=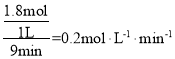 ������ƽ�ⳣ���Ķ��壬�¶�Ϊt1ʱ���÷�Ӧ��ƽ�ⳣ��K=
������ƽ�ⳣ���Ķ��壬�¶�Ϊt1ʱ���÷�Ӧ��ƽ�ⳣ��K=![]() ����Ϊ��0.2mol��L-1��min-1��16.2��
������0.2mol��L-1��min-1��16.2��
II.��3����ͼ1��֪��CO2�ڴ���ͭ�ı������ת���������ɵIJ�����C2H4�����ݷ�����������ԭ��Ӧ�Ĺ�ϵ���У�2CO2��C2H4��12e-����ֱ�Ӵ��ݵĵ������ʵ���Ϊ2mol����μӷ�Ӧ��CO2�����ʵ���Ϊ0.33mol����Ϊ��0.33mol��
��4����ͼ2��֪��Cu���Դ�ĸ���������Cu�缫Ϊ���ص�������������ԭ��Ӧ��CO2�õ�������CH4���缫��Ӧ����ʽΪ��CO2+8e-+6H2O=CH4+8OH-����Ϊ��CO2+8e-+6H2O=CH4+8OH-��
III.��5��ͭ���Ӵ��ŷű������ʵ���Ũ��Ϊ![]() ������Ksp(CuS)=1��10-36����֪Ҫʹͭ���ӵ�Ũ�ȷ����ŷű�����Һ�е������ӵ����ʵ���Ũ��Ϊ
������Ksp(CuS)=1��10-36����֪Ҫʹͭ���ӵ�Ũ�ȷ����ŷű�����Һ�е������ӵ����ʵ���Ũ��Ϊ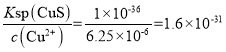 mol/L����Ϊ��
mol/L������![]() ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����֪ij��ѧ��Ӧ��ƽ�ⳣ������ʽΪK=![]() ���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ��
���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ��
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
�����й���������ȷ���ǣ�������
A. �÷�Ӧ�Ļ�ѧ����ʽ��CO��g��+H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
B. ������Ӧ������Ӧ�Ƿ��ȷ�Ӧ
C. ����1L���ܱ�������ͨ��CO2��H2��1mol��5min���¶����ߵ�830�棬��ʱ���CO2Ϊ0.4molʱ���÷�Ӧ�ﵽƽ��״̬
D. ��ƽ��Ũ�ȷ������й�ϵʽ��![]() �����ʱ���¶�Ϊ1000��
�����ʱ���¶�Ϊ1000��