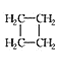题目内容
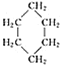
【题目】环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下表是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂)。
结构简式 |
|
|
|
键线式 |
|
|
|
①![]() +H2
+H2![]()
![]()
②![]() +H2
+H2![]()
![]()
③![]() +H2
+H2![]()
![]()
④![]() +KMnO4
+KMnO4![]()
![]() +
+![]() +Mn2+
+Mn2+
回答下列问题:
(1)环烷烃与___________是同分异构体。
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是______(填名称),判断依据为_________。
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件反应,其化学方程式为(不需注明反应条件)____________。
(4)写出鉴别环丙烷与丙烯的一种方法:试剂___________;现象与结论 __________。
【答案】同碳原子数的烯烃 环丙烷 反应所需条件(温度)要求最低 ![]() +HBr→
+HBr→![]() 酸性KMnO4溶液 能使酸性KMnO4溶液褪色的是丙烯,不褪色的是环丙烷
酸性KMnO4溶液 能使酸性KMnO4溶液褪色的是丙烯,不褪色的是环丙烷
【解析】
(1)由表中结构简式可知环烷烃的通式为CnH2n,显然与具有相同碳原子数的烯烃互为同分异构体,故答案为:相同碳原子数的烯烃(或相对分子质量相同的烯烃);
(2)比较①~③的反应条件(温度)知,①反应温度最低,故环丙烷最易发生开环加成反应,故答案为:环丙烷;反应温度最低;
(3)根据题干加成反应的信息:环结构变为链结构,不难写出所求反应的方程式为:![]() +HBr→
+HBr→![]() ,故答案为:
,故答案为:![]() +HBr→
+HBr→![]() ;
;
(4)由反应④知环烷结构不与KMnO4(H+)反应,而碳碳双键易被氧化,故用酸性KMnO4溶液可将环丙烷和丙烯区别开,故答案为:酸性高锰酸钾溶液;使酸性高锰酸钾溶液退色的是丙烯,另一种是环丙烷(或溴水,使溴水发生加成反应退色的是丙烯)。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】NiSO46H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废液(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得。工艺流程如图:
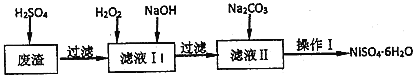
已知: 25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示。
Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
注:NiCO3是一种不溶于水易溶于强酸的沉淀。
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有________。
A.升高反应温度 B.增大压强 C.在反应过程中不断搅拌
(2)在滤液I中加入6%的H2O2,其作用是__________(用离子方程式表示);加入NaOH调节pH的范围是_________,为了除去溶液中的_________离子。
(3)检验Ni2+已完全沉淀的实验方法是_________________。
【题目】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
| IA | 0 | |||||||
1 | ① | II A | III A | IV A | V A | VI A | VIIA | ||
2 | ② | ③ | |||||||
3 | ④ | ⑤ | ⑥ | ||||||
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为 ;
(2)②、③两元素的原子半径较大的是______________(填元素符号);
(3)④和⑤两种元素的金属性较强的是 (填元素符号);
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式 。