题目内容
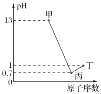
【题目】25℃时,向20mL0.1mol/LH2R溶液中滴加0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知pKa=-lgKa,二元弱酸H2R的pKa1=1.89,pKa2=7.21。下列有关说法不正确的是
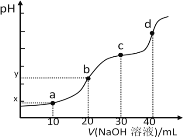
A.溶液的导电性:点a弱于点b
B.离子浓度c(R2-):点c大于点d
C.H2R+R2-=2HR-平衡常数>105,反应趋于完全
D.点b时,y<7且![]() <1
<1
【答案】BD
【解析】
A. a点的溶质为等物质的量的H2R、NaHR,b点的溶质完全变为NaHR,a→b弱电解质H2R变为强电解质NaHR,溶液的导电性增强,故A正确;
B. c点的溶液是0.02 mol/L NaHR、0.02 mol/L Na2R 的混合液,d点是0.033mol/L的Na2R溶液,所以离子浓度c(R2-):点c小于点d,故B错误;
C. H2R+R2-=2HR-平衡常数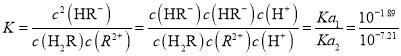 >105,反应趋于完全,故C正确;
>105,反应趋于完全,故C正确;
D. b点的溶质为NaHR,HR- 水解小于电离,溶液呈酸性, ![]() >1,故D错误;
>1,故D错误;
选BD。

练习册系列答案
相关题目