题目内容
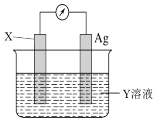
【题目】水系钠离子电池安全性能好、价格低廉、对环境友好,有着巨大的市场前景。某钠离子电池工作原理如图,电池总反应为:2NaFePO4F+Na3Ti2(PO4)3![]() 2Na2FePO4F+NaTi2(PO4)3
2Na2FePO4F+NaTi2(PO4)3
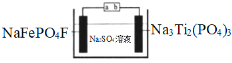
下列说法错误的是( )
A.充电时,a接电源负极
B.放电时,溶液中的Na+在NaFePO4F电极上得电子被还原
C.充电时,阴极上的电极反应为NaTi2(PO4)3+2Na++2e﹣=Na3Ti2(PO4)3
D.理论上,该电池在充电或放电过程中溶液中的c(Na+)不变
【答案】AB
【解析】
根据电池总反应,放电时NaFePO4F→Na2FePO4F,Fe元素化合价由+3降低为+2,NaFePO4F为正极;放电时Na3Ti2(PO4)3→NaTi2(PO4)3,Ti元素化合价由+3升高为+4,Na3Ti2(PO4)3是负极。
A. a是原电池正极,充电时,原电池的正极作阳极,a接电源正极,故A错误;
B. 放电时, NaFePO4F电极上的Fe元素化合价由+3降低为+2,Fe元素被还原,故B错误;
C. 充电时,阴极发生还原反应,阴极上的电极反应为NaTi2(PO4)3+2Na++2e﹣=Na3Ti2(PO4)3,故C正确;
D. 根据总反应式2NaFePO4F+Na3Ti2(PO4)3![]() 2Na2FePO4F+NaTi2(PO4)3,硫酸钠、水不参与反应,该电池在充电或放电过程中溶液中的c(Na+)不变,故D正确;
2Na2FePO4F+NaTi2(PO4)3,硫酸钠、水不参与反应,该电池在充电或放电过程中溶液中的c(Na+)不变,故D正确;
选AB。

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目