题目内容
18.下列说法正确的是( )| A. | 丙烷具有同分异构体 | |
| B. | C2H4是最简单的烯烃 | |
| C. | CH2Cl2的结构有2种说明CH4是正四面体分子 | |
| D. | 因为乙烷不具有同分异构现象,所以二氯乙烷也不具有同分异构现象 |
分析 A.碳原子数小于等于3的烷烃没有同分异构体;
B.最简单的烯烃是乙烯;
C.如果甲烷是正方形的平面结构,CH2Cl2有两种结构:相邻或者对角线上的氢被Cl取代,如果是正四面体结构,CH2Cl2只有一种结构;
D.二氯乙烷中两个氯原子可以在同一个碳原子上,也可以在不同的碳原子上.
解答 解:A.丙烷中碳原子数等于3,没有具有同分异构体,故A错误;
B.乙烯(分子式为C2H4)是最简单的烯烃,故B正确;
C.CH2Cl2的结构有1种说明CH4是正四面体分子,故C错误;
D.乙烷不具有同分异构现象,但二氯乙烷具有同分异构现象:二氯乙烷中两个氯原子可以在同一个碳原子上,也可以在不同的碳原子上,故D错误;
故选B.
点评 本题考查常见有机化合物的结构,题目难度中等,注意CH2Cl2只代表一种物质,可以证明甲烷分子是空间正四面体结构,而不是平面正方形结构.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
6.下列化学方程式中,书写不正确的是( )
| A. | 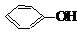 +NaOH→ +NaOH→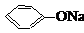 +H2O +H2O | B. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | ||
| C. | CH2=CH2+H2O→CH3CH2OH | D. | CH4+Cl2→CH2Cl2+H2 |
10.研究碳氧化物的利用对促进低碳社会的构建具有重要的意义.
(1)二氧化碳合成甲醇是碳减排的新方向,已知:
①2H2(g)+O2(g)=2H2O(g)△H=-484kJ•mol-1
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-677kJ•mol-1
以CO2和H2为原料合成甲醇的热化学方程式为CO2(g)+3H2 (g)=CH3OH(g)+H2O(g)△H=-49kJ•mol-1,
已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示.则平衡状态由A变到B时,平衡常数K(A)=K(B)(填“>”、“<”或“=”).
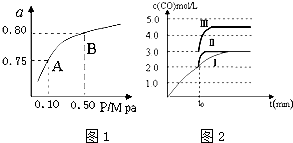
(3)判断反应③△H<0;△S<0(填“>”“=”或“<”)
在500℃、2L的密闭容器中,进行反应③,测得某时刻H2、CO2、CH3OH、H2O的物质的量分别为6mol、2mol、10mol、10mol,此时v(正)>v(逆) (填“>”“=”或“<”)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)?H2O (g)+CO(g),已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积快速压缩至2L.利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池负极的电极反应式SO2-2e-+2H2O═SO42-+4H+.
(4)利用Na2SO3溶液充分吸收SO2制得NaHSO3溶液.
常温时吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:
以下离子浓度关系的判断正确的是C
A.NaHSO3溶液中c(H+)<c(OH-)
B.Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c(HSO3-)>c(SO32-)>c(OH-)=c(H+)
D.当n(SO32-):n(HSO3-)=1:1时,c(Na+)=c(HSO3-)+2c(SO32-).
(1)二氧化碳合成甲醇是碳减排的新方向,已知:
①2H2(g)+O2(g)=2H2O(g)△H=-484kJ•mol-1
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-677kJ•mol-1
以CO2和H2为原料合成甲醇的热化学方程式为CO2(g)+3H2 (g)=CH3OH(g)+H2O(g)△H=-49kJ•mol-1,
已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
| 化学反应 | 平衡常数 | 温度(℃) | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O (g) | K3 | ||

(3)判断反应③△H<0;△S<0(填“>”“=”或“<”)
在500℃、2L的密闭容器中,进行反应③,测得某时刻H2、CO2、CH3OH、H2O的物质的量分别为6mol、2mol、10mol、10mol,此时v(正)>v(逆) (填“>”“=”或“<”)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)?H2O (g)+CO(g),已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积快速压缩至2L.利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池负极的电极反应式SO2-2e-+2H2O═SO42-+4H+.
(4)利用Na2SO3溶液充分吸收SO2制得NaHSO3溶液.
常温时吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| PH | 8.2 | 7.2 | 6.2 |
A.NaHSO3溶液中c(H+)<c(OH-)
B.Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c(HSO3-)>c(SO32-)>c(OH-)=c(H+)
D.当n(SO32-):n(HSO3-)=1:1时,c(Na+)=c(HSO3-)+2c(SO32-).