题目内容
【题目】乙醇分子中不同的化学键如图:关于乙醇在各种反应中断裂键的说法不正确的是

A. 乙醇和钠反应,键①断裂
B. 在铜催化下和O2反应,键①③断裂
C. 浓硫酸作用下加热至170℃时的反应,键②⑤断裂。
D. 浓硫酸作用下加热至140℃时的反应,键①⑤断裂
【答案】D
【解析】
乙醇的官能团为-OH,可发生取代反应、氧化反应和消去反应,可与钠反应,结合官能团的性质判断可能的共价键的断裂方式。
A项、乙醇和钠反应生成乙醇钠和氢气时,羟基上O-H键断裂,即键①断裂,故A正确;
B项、乙醇发生催化氧化生成乙醛时,连接羟基碳原子上的C-H键和羟基中O-H键断裂,即键①和键③断裂,故B正确;
C项、乙醇浓硫酸作用下加热至170℃发生消去反应生成乙烯时,与羟基相连碳原子上的C-O键和与羟基相邻的碳原子上的C-H键断裂,即键②⑤断裂,故C正确;
D项、乙醇浓硫酸作用下加热至140℃发生分子间脱水反应生成乙醚反应时,一个醇分子断氢氧键,另一个醇分子断碳氧键,即①或②断裂,故D错误。
故选D。

【题目】利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
某工厂对制革工业污泥中Cr元素的回收与再利用工艺如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
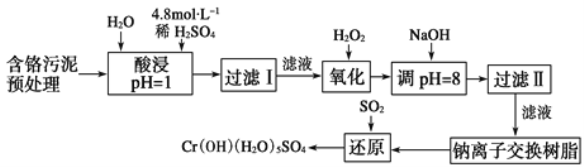
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9(>9溶解) |
(1) 酸浸时,为了提高浸取率可采取的措施是____(至少写两条)。
(2)H2O2的作用是_____。
(3)调pH=8是为了除去___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(4)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(5)已知以下氧化还原反应方程式(未配平):Na2Cr2O7+SO2+H2O=Cr(OH)(H2O)5SO4+Na2SO4;以上反应各物质的配平系数依次为___。每生成1 mol Cr(OH)(H2O)5SO4转移电子的数目为___。