题目内容
A、B、C、D四种化合物,其焰色反应通过蓝色钴玻璃观察均为紫色.A、B、C和盐酸反应均生成D,B和C反应可生成A;在B溶液中通入一种无色无味气体时,适量时得A,过量时得C.写出化学式:A________;B________;C________;D________.有关反应的离子方程式:(1)C+盐酸:________;(2)B→A:________.
答案:
解析:
提示:
解析:
|
A:K2CO3,B:KOH,C:KHCO3,D:KCl (1) |
提示:
|
提示:解答本题要求熟悉物质之间的反应.焰色反应通过蓝色钴玻璃观察均为紫色,说明四种物质阳离子相同为K+.A、B、C与盐酸均生成同种物质D,D应为KCl,根据复分解反应条件,三种物质与盐酸反应的另一种产物是H2O或气体,推断A、B、C可能是KOH、K2CO3、KHCO3.B、C反应生成A,而KOH能和KHCO3生成K2CO3,推断A为K2CO3.B可能为KOH或者KHCO3.其中KOH溶液中通入无色无味气体CO2适量时得K2CO3,过量时生成KHCO3,确定B为KOH,则C为KHCO3. |

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
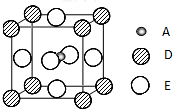 (2010?泰州三模)已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大.A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2-离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2.
(2010?泰州三模)已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大.A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2-离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2.