题目内容
15.X、Y、Z、W、Q为4种短周期元素,在周期表位置如图.下列说法正确的是( )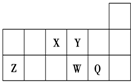
| A. | 元素X与元素Z的最高正化合价之和的数值等于8 | |
| B. | 原子半径的大小顺序为:Y>Z | |
| C. | 离子Y2-和Z3+的核外电子总数和电子层数都不相同 | |
| D. | 元素W的单质比Q的熔点低 |
分析 X、Y、Z、W、Q都是短周期元素,根据元素在周期表中的位置可知,X是N元素、Y是O元素、Z是Al元素、W是S元素、Q是Cl元素,结合元素周期律与元素化合物性质解答.
解答 解:X、Y、Z、W、Q都是短周期元素,根据元素在周期表中的位置可知,X是N元素、Y是O元素、Z是Al元素、W是S元素、Q是Cl元素.
A.元素X与元素Z的最高正化合价分别为+3、+5,二者最高正化合价之和的数值等于8,故A正确;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Z>Y,故B错误;
C.离子O2-和Al3+的核外电子总数均为10,均有2个电子层,故C错误;
D.常温下,硫单质为固体,而氯气为气体,硫的熔点高于氯气,故D错误,
故选:A.
点评 本题考查位置结构性质的相互关系及应用,题目难度不大,注意掌握元素周期表的结构和元素周期律的递变规律.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
6.有A、B两种烃,其相关信息如下:
回答下列问题:
(1)烃A的实验式是CH;
(2)烃A的结构简式是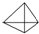 ;
;
(3)烃B的三种二溴代物的结构简式为CHBr2CH(CH3)2、CH2BrCBr(CH3)2、CH2BrCH(CH3)CH2Br;
(4)烃C为烃B的同系物,常温下为气态且只有一种一溴代物,则烃C的一溴代物的结构简式为CH3Br或CH3CH2Br或(CH3)3CCH2Br(填一种即可).
| A | ①完全燃烧的产物中n(CO2):n(H2O)=2:1 ②28<M (A)<60 ③不能使溴的四氯化碳溶液褪色 ④一氯代物只有一种结构 |
| B | ①饱和链烃,通常情况下呈气态 ②有同分异构体 ③二溴代物有三种 |
(1)烃A的实验式是CH;
(2)烃A的结构简式是
 ;
;(3)烃B的三种二溴代物的结构简式为CHBr2CH(CH3)2、CH2BrCBr(CH3)2、CH2BrCH(CH3)CH2Br;
(4)烃C为烃B的同系物,常温下为气态且只有一种一溴代物,则烃C的一溴代物的结构简式为CH3Br或CH3CH2Br或(CH3)3CCH2Br(填一种即可).
3.下列反应的离子方程式书写正确的是( )
| A. | 氯化亚铁溶液和氯气反应:Fe2++Cl2═Fe3++2Cl- | |
| B. | 大理石和盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 碳酸氢钠溶液和稀硝酸反应:HCO3-+H+═H2↑+CO32- | |
| D. | 盐酸和氢氧化钾溶液反应:H++OH-═H2O |
10.下列物质中,属于电解质的是( )
| A. | Cl2 | B. | NaNO3 | C. | SO2 | D. | 硫酸溶液 |
20.有机物:①正己烷 ②2-甲基丁烷 ③2-甲基丙烷 ④丙烷 ⑤乙烷它们的沸点按由高到低的顺序排列正确的是( )
| A. | ①>②>③>④>⑤ | B. | ⑤>④>③>②>① | C. | ①>②>④>③>⑤ | D. | ①>②>③>⑤>④ |
4.下列说法不正确的是 ( )
| A. | 验证淀粉水解产物时,在淀粉溶液中加几滴稀硫酸,水浴5min,加入新制银氨溶液 | |
| B. | 煤油可由石油分馏获得,可用作燃料和保存少量的金属钠 | |
| C. | 向2mLl0%NaOH溶液中滴入2%CuS04溶液的4-6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾,则有砖红色沉淀出现 | |
| D. | 植物油能使溴的四氯化碳溶液褪色,盛过油脂的试管用碱液洗涤 |
 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: