题目内容
【题目】X、Y、Z三种物质有如图所示转化关系,其中X与稀盐酸不反应:
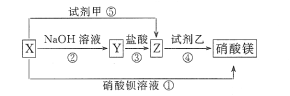
(1)根据上述转化关系,推断下列物质的化学式: X_____,Y_____,Z____,试剂甲____,试剂乙____。
(2)写出上述①~⑤步反应的离子方程式:
①____________________________________________。
②____________________________________________。
③____________________________________________。
④____________________________________________。
⑤____________________________________________。
【答案】MgSO4 Mg(OH)2 MgCl2 BaCl2 AgNO3 Ba2++ SO42—===BaSO4↓ Mg2++2OH===Mg(OH)2↓ Mg(OH)2 +2H+===Mg2++2H2O Ag+ +Cl===AgCl↓ Ba2++ SO42—===BaSO4↓
【解析】
(1)反应①,X能与硝酸钡反应生成硝酸镁,即X中含有Mg元素,因为X不能与盐酸反应,因此X为MgSO4,MgSO4与NaOH反应生成Mg(OH)2,即Y为Mg(OH)2,Z为MgCl2,X与试剂甲反应生成MgCl2,则试剂甲为BaCl2,MgCl2与试剂乙反应生成硝酸镁,则试剂乙为AgNO3;
(2)①发生化学反应为MgSO4+Ba(NO3)2=Mg(NO3)2+BaSO4↓,即离子方程式为Ba2++SO42-=BaSO4↓,
②反应②的方程式为MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,其离子方程式为Mg2++2OH-=Mg(OH)2↓,
③氢氧化镁与盐酸发生中和反应,即离子方程式为Mg(OH)2+2H+=Mg2++2H2O,
④MgCl2与AgNO3发生复分解反应,即离子方程式为Cl-+Ag+=AgCl↓,
⑤发生复分解反应,其离子方程式为Ba2++SO42-=BaSO4↓。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案【题目】钛被誉为“21世纪的金属”,可呈现多种化合价。其中以+4价的Ti最为稳定。
(1)基态Ti原子的价电子轨道表示式为_______________。
(2)已知电离能:I2(Ti)=1310kJ/mol,I2(K)=3051kJ/mol。I2(Ti)<I2(K),其原因为________。
(3)钛某配合物可用于催化环烯烃聚合,其结如图所示:
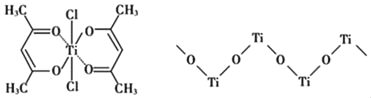
①钛的配位数为_____,碳原子的杂化类型_____。
②该配合物中存在的化学键有___________(填字母标号)。
a.离子健 b.配位键 c.金属健 d.共价键 e.氢键
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如上图所示,该阳离子化学式为________,阴离子SO42—的空间构型为____。
(5)钛与卤素形成的化合物熔沸点如下表所示:
TiCl4 | TiBr4 | TiI4 | |
熔点/℃ | ﹣24.1 | 38.3 | 155 |
沸点/℃ | 136.5 | 233.5 | 377 |
分析 TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是:_____。
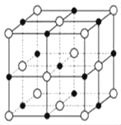
(6)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度ρg/cm3,阿伏加德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为________pm.(用含ρ、NA的代数式表示)