题目内容
(1)将AgNO3溶液分别与HCl、NaCl、KCl溶液混合,均有 产生,它们的离子方程式是 ,说明离子反应方程式不仅表示一定物质间的 ,而且表示了 离子反应.
(2)某电解质溶液中,可能含有大量的H+、Cu2+、Ag+、CO32-、OH-、Cl-,则该溶液中一定含有的离子是 ,一定没有的离子是 ;还需进一步确认的离子是 ,确认的方法为 .
(2)某电解质溶液中,可能含有大量的H+、Cu2+、Ag+、CO32-、OH-、Cl-,则该溶液中一定含有的离子是
考点:物质的检验和鉴别的基本方法选择及应用,离子方程式的书写
专题:物质检验鉴别题
分析:(1)均生成AgCl白色沉淀,离子反应可表示一类物质的反应,也可表示某一个具有的离子反应;
(2)H+、Cu2+、Ag+均与OH-、CO32-反应,则溶液中一定存在Cl-,由Ag++Cl-═AgCl↓可知,一定没有Ag+,H+、Cu2+至少有1个,则溶液中一定不存在OH-、CO32-,以此来解答.
(2)H+、Cu2+、Ag+均与OH-、CO32-反应,则溶液中一定存在Cl-,由Ag++Cl-═AgCl↓可知,一定没有Ag+,H+、Cu2+至少有1个,则溶液中一定不存在OH-、CO32-,以此来解答.
解答:
解:(1)AgNO3溶液分别与HCl、NaCl、KCl溶液混合,均发生Ag++Cl-═AgCl↓则观察到白色沉淀生成,说明离子反应方程式不仅表示一定物质间的某一具体反应,而且表示可同一类型的离子反应,故答案为:白色沉淀;Ag++Cl-═AgCl↓;某一具体反应;同一类型;
(2)(2)H+、Cu2+、Ag+均与OH-、CO32-反应,则溶液中一定存在Cl-,由Ag++Cl-═AgCl↓可知,一定没有Ag+,H+、Cu2+至少有1个,则溶液中一定不存在OH-、CO32-,进一步确认的离子是H+、Cu2+,确认方法为观察溶液颜色,如为蓝色则有Cu2+,若加CaCO3粉末,若有气泡产生,则有H+(或测定pH是否小于7),
故答案为:Cl-;Ag+、OH-、CO32-;H+、Cu2+;观察溶液颜色,如为蓝色则有Cu2+,若加CaCO3粉末,若有气泡产生,则有H+(或测定pH是否小于7).
(2)(2)H+、Cu2+、Ag+均与OH-、CO32-反应,则溶液中一定存在Cl-,由Ag++Cl-═AgCl↓可知,一定没有Ag+,H+、Cu2+至少有1个,则溶液中一定不存在OH-、CO32-,进一步确认的离子是H+、Cu2+,确认方法为观察溶液颜色,如为蓝色则有Cu2+,若加CaCO3粉末,若有气泡产生,则有H+(或测定pH是否小于7),
故答案为:Cl-;Ag+、OH-、CO32-;H+、Cu2+;观察溶液颜色,如为蓝色则有Cu2+,若加CaCO3粉末,若有气泡产生,则有H+(或测定pH是否小于7).
点评:本题考查离子的检验及离子反应,为高频考点,把握离子反应的实质、离子共存、离子反应为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某溶液中由水电离产生的C(H+)=1×10-10mol/L,该溶液的溶质不可能是( )
| A、KOH |
| B、Na2CO3 |
| C、HClO4 |
| D、Na HSO4 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是( )
| A、标准状况下,1.12L的SO3所含的原子数约为0.2×6.02×1023 |
| B、1mol MgCl2中含有的离子数约为2×6.02×1023 |
| C、1.8g的NH4+离子中含有的电子数约为6.02×1023 |
| D、2.4g金属镁变为镁离子时失去的电子数约为0.1×6.02×1023 |
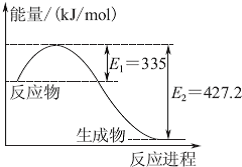 (1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
(1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol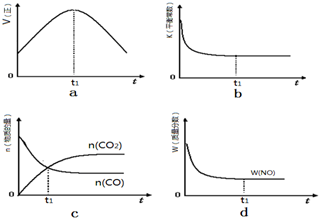
 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.