题目内容
16.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述不正确的是( )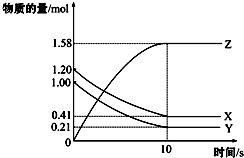
| A. | 反应开始到10s,用Z表示的反应速率为0.079mol/(L•s) | |
| B. | 该反应的方程式为:X(g)+Y(g)?2 Z(g) | |
| C. | 反应开始到10s时,Y的转化率为79.0% | |
| D. | 反应进行到10s时,该反应达到限度且各组分浓度相等 |
分析 根据图象的曲线变化判断物质的量的变化进而判断反应平衡所需时间以及反应速率、转化率的计算,根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式.
A、反应速率v=$\frac{△c}{△t}$;
B、由图象可以看出,反应中x、Y的物质的量减少,应为反应物,z的物质的量增多,应为生成物,当反应进行到3min时,△n(X)=0.79mol,△n(Y)=0.79mol,△n(Z)=1.58mol,则△n(X):△n(Y):△n(Z)=1:1:2,参加反应的物质的物质的量之比等于化学计量数之比;
C、转化率=$\frac{消耗量}{起始量}$×100%;
D、平衡标志是指正逆反应速率相同,各组分的含量和浓度保持不变.
解答 解:A.反应开始到10s,用Z表示的反应速率$\frac{\frac{1.58mol}{2L}}{10s}$=0.079mol/(L•s),故A正确;
B.由图象可以看出,反应中x、Y的物质的量减少,应为反应物,z的物质的量增多,应为生成物,当反应进行到3min时,△n(X)=0.79mol,△n(Y)=0.79mol,△n(Z)=1.58mol,
则△n(X):△n(Y):△n(Z)=1:1:2,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为X(g)+Y(g)?2Z(g),故B正确;
C.反应开始到10s时,Y的转化率为$\frac{1.0mol-0.21mol}{1.0mol}$×100%=79%,故C正确;
D.根据图象可知在10s后,X、Y、Z的物质的量不再随时间的变化而变化,即反应达到平衡状态,各组分的浓度不相同,故D错误;
故选D.
点评 本题考查化学平衡图象问题,题目难度不大,注意分析图象中各物理量的变化曲线,把握相关物理量的计算.

 阅读快车系列答案
阅读快车系列答案| A. | CH4、NH3、HF | B. | OH-、F-、NH3 | C. | H3O+、NH4+、Mg2+ | D. | O2-、OH-、NH2- |
| A. | 原子半径依次增大 | B. | 气态氢化物的稳定性依次减弱 | ||
| C. | 气态氢化物水溶液的酸性依次减弱 | D. | 气态氢化物的还原性依次增强 |
| A. | 从氟到碘,其氢化物的稳定性逐渐减弱 | |
| B. | 因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 | |
| C. | 第三周期从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 | |
| D. | 氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 |
| A. | 不改变 | B. | 逐渐减小 | C. | 逐渐增大 | D. | 先减小,后增大 |
| A. | ①②③ | B. | ①④ | C. | ①③ | D. | ①②③④ |
| A. | ①②④⑤③⑥ | B. | ①⑤④②①③⑥ | C. | ①⑤④②③⑥ | D. | ①②④⑤①③⑥ |