题目内容
【题目】按要求填空
(1)水被称为“生命之源”,为了给某地区的人民寻找合适的饮用水源,某化学小组对附近山上的泉水进行了分析,结果显示水体硬度超标,其水体中主要含Ca2+、Mg2+、HCO3﹣和Cl﹣ . 则该水源属于(填“暂时”或“永久”)硬水,可通过加热煮沸来降低水体的硬度,水体中的Ca2+、Mg2+在加热煮沸后将分别转化为、形成水垢.
(2)我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献.生产流程如图: 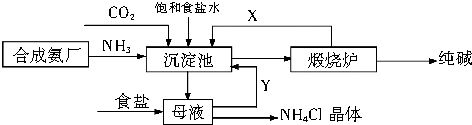
①向沉淀池中通入NH3和CO2气体时,正确的顺序是 .
②流程图中X表示的物质是
(3)贵州铝厂是目前我国最大的电解铝生产基地.所需生产原料Al2O3可以从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取,其工艺流程如下: 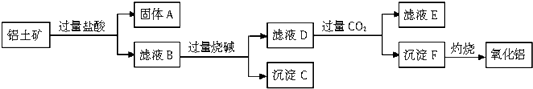
请回答下列问题:
①固体A是 , 滤液E中含有的溶质是
②已知298K时,Mg(OH)2的容度积常数Ksp=5.6×10﹣12 , 取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡时,测得pH=13.0,则此时溶液中的c(Mg2+)=molL﹣1 .
【答案】
(1)暂时;CaCO3;Mg(OH)2
(2)先通入NH3至饱和后再通入CO2至饱和;CO2
(3)SiO2;NaCl和NaHCO3;5.6×10﹣10
【解析】解:(1)根据水的硬度是由钙和镁的碳酸氢盐或氯化物等引起的,这种硬度叫做暂时硬度,加热煮沸后会生成碳酸钙和氢氧化镁沉淀,
所以答案是:暂时;CaCO3;Mg(OH)2;
(2.)在联合制碱法中,联合制碱法包括两个过程:第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO3微小晶体,再煅烧制得纯碱产品,放出的二氧化碳气体可回收循环使用,其滤液是含有氯化铵和氯化钠的溶液,向含有氯化铵和氯化钠的滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品,
①由于氨气易溶于水,所以向沉淀池中通入NH3和CO2气体时,正确的顺序是先通入NH3至饱和后再通入CO2至饱和,
所以答案是:先通入NH3至饱和后再通入CO2至饱和;
②根据上面的分析可知,流程图中X表示的物质是CO2 ,
所以答案是:CO2
(3.)由工艺流程甲可知,向铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中加入盐酸,铝土矿与盐酸反应得固体A为滤液B,则固体A为SiO2 , 滤液B含有氯化铝、氯化铁、氯化镁等,滤液中加入过量的NaOH,可推知沉淀C为氢氧化铁、氢氧化镁,滤液D含有偏铝酸钠、氯化钠、NaOH,所以向滤液D中通入过量二氧化碳,生成氢氧化铝沉淀与碳酸氢钠,沉淀F为Al(OH)3 , 滤液E中含有NaCl、NaHCO3 , 氢氧化铝灼烧得氧化铝,
①根据上面的分析可知,固体A是SiO2 , 滤液E中含有的溶质是 NaCl和NaHCO3 ,
所以答案是:SiO2; NaCl和NaHCO3;
②溶液的pH=13.0时,溶液中c(OH﹣)=0.1mol/L,由氢氧化镁溶度积常数计算镁离子浓度,Ksp=c(Mg2+)c2(OH﹣)=5.6×10﹣12 , 代入计算得到c(Mg2+)=5.6×10﹣10 mol/L,
所以答案是:5.6×10﹣10 .

【题目】化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
(1)已知:FeO(s)+CO(g)FeO(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如右表:
T(K) | 938 | 1100 |
K | 0.68 | 0.40 |
①该反应平衡常数的表达式是 .
②在体积固定的密闭容器中该反应达到平衡状态后,升高温度混合气体的平均相对分子质
量(填“增大”、“减小”或“不变”)曰该反应正反应是反应(填“吸热”或“放热”).
(2)常温下,下列溶液的浓度均为0.1molL﹣1 , 测得溶液pH值如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
①由表中数据分析,上述溶质中的阴离子水解程度最小的是(填离子符号).
②由表中数据分析,0.01molL﹣1的下列溶液,酸性最弱的是(填编号).
A、H2CO3 B、HClO C、C6H5OH D、CH3COOH
③向氯水中加入少量的碳酸钠,可以增加氯水中HClO的浓度.为什么? . (请结合化学反应简要说明)