题目内容
【题目】某工厂排放的工业废水中含Fe3+、Al3+、Cu2+ , 为了减少环境污染,变废为宝,利用废铁屑制得Fe2O3、Al2O3和金属Cu,过程如下. 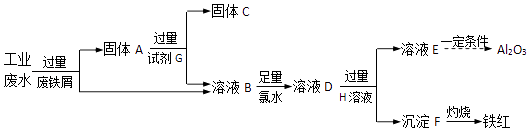
(1)固体A的成分是(填化学式).
(2)溶液B中的金属阳离子有 .
(3)B→D反应的离子方程式是 .
(4)试剂G是(填名称).
(5)溶液E焰色反应呈黄色,试剂H是 .
【答案】
(1)Fe、Cu
(2)Fe3+、Al3+、Fe2+
(3)2Fe2++Cl2=2Fe3++2Cl﹣
(4)盐酸
(5)NaOH
【解析】解:(1)根据流程图中可以知道,完成回收铁红、Al2O3和金属Cu,先加过量铁粉,2Fe3++Fe═3 Fe2+ , 铁在金属活动顺序表中排在铜的前面,所以铁粉把铜置换出来,Cu2++Fe=Fe2++Cu,过滤得到Fe、Cu, 所以答案是:Fe、Cu;(2)金属铁可以和铁离子、铜离子之间反应,过滤所得溶液B中含有Al3+、Fe2+ , 所以答案是:Fe3+、Al3+、Fe2+;(3)B→D反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl﹣ , 所以答案是:2Fe2++Cl2=2Fe3++2Cl﹣;(4)由上述分析可知,G为盐酸,所以答案是:盐酸;(5)分离Al3+、Fe2+ , 需加强碱,氢氧化铝既可以和强酸反应还可以和强碱反应,溶液E焰色反应呈黄色说明含有钠离子,说明试剂H是氢氧化钠,
所以答案是:NaOH.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
