��Ŀ����
����Ŀ����֪ij�ֶ�������ӵ�ع���ʱ��ӦΪ��LixCn + Li(1-x)CoO2 == LiCoO2 + nC�������ͼ��ʾ������˵������ȷ����
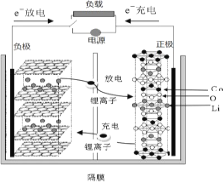
A.�ŵ�ʱ��̼���ϼ�ʧȥ���ӣ�����������Ӧ�����Ӿ����·��Li+���ڵ�·ͬʱ��������
B.�ŵ�ʱ������ӦΪ�� Li(1-x)CoO2 + xLi+ + xe- = LiCoO2
C.���ʱ�� Li+�Ӹ����ѳ�����Ƕ������
D.����Ӷ��ε��������֮���ŵ�ʱ�������� Li+�ķ�Ӧ�����и���Ӧ
���𰸡�C
��������
�ŵ�ʱ�ķ�ӦΪLixCn + Li(1-x)CoO2 == LiCoO2 + nC��CoԪ�صĻ��ϼ۽��ͣ�LiԪ�صĻ��ϼ����ߣ�ԭ����и�������������Ӧ����ӦʽΪ��LixCn-xe-= xLi++ nC������������ԭ��Ӧ����ӦʽΪ��Li(1-x)CoO2 + xLi+ + xe- = LiCoO2�����ɷŵ�ʱ�ķ�Ӧ�������ʱ�ķ�Ӧ��
A���ŵ�ʱ��̼���ϼ�Ϊ����������������Ӧ�����Ӿ����·��Li+���ڵ�·ͬʱ������������A��ȷ��
B��������������֪��CoԪ�صĻ��ϼ۽��ͣ�������ӦʽΪ��Li(1-x)CoO2 + xLi+ + xe- = LiCoO2����B��ȷ��
C�����ʱ��Li+Ӧ�������ѳ���Ƕ����������C����
D����������������Ӧ��֪������Ӷ��ε��������֮���ŵ�ʱ�������� Li+�ķ�Ӧ�����и���Ӧ����D��ȷ��
��ѡC��

 ��У����ϵ�д�
��У����ϵ�д�