题目内容
15.在一恒温恒容的密闭容器中,放入一定量的甲醇,发生反应:CH3OH(l)?CO(g)+2H2(g).以下可以作为该反应达到平衡状态的判断依据为( )| A. | 容器内气体密度保持不变 | |
| B. | 气体的平均相对分子质量保持不变 | |
| C. | CO的体积分数保持不变 | |
| D. | CO与H2的物质的量之比保持1:2不变 |
分析 当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,根据密度和平均相对分子质量的公式进行分析解答该题.
解答 解:A.在恒容容器中,体积不变,由CH3OH(l)?CO(g)+2H2(g)反应可得反应前后气体质量在变,所以密度保持不变,证明达到了化学平衡状态,故A正确;
B.由于甲醇为液体,气体的组成一直不变,CO与氢气的物质的量之比一直是1:2,则平均相对分子质量一直不变,所以平均相对分子质量保持不变不能证明达到了化学平衡状态,故B错误;
C.由于甲醇为液体,气体的组成一直不变,CO与氢气的物质的量之比一直是1:2,所以CO的体积分数一直不变,所以CO的体积分数保持不变,不能证明达到了化学平衡状态,故C错误;
D.由于甲醇为液体,气体的组成一直不变,CO与氢气的物质的量之比一直是1:2,所以不能证明达到了化学平衡状态,故D错误.
故选:A.
点评 本题考查了化学平衡状态的判断,难度不大,注意:只有反应前后改变的物理量才能作为判断化学平衡的依据,反应前后不改变的物理量不能作为化学平衡的判断依据.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
6.下列有关物质性质或应用的说法正确的是( )
| A. | 二氧化锰具有强氧化性,能将双氧水氧化为氧气 | |
| B. | Zn具有氧化性和导电性,可用作锌锰干电池的负极材料 | |
| C. | 炭具有强还原性,高温下能将二氧化硅还原为硅 | |
| D. | 二氧化硫具有漂白性,与氯水混合使用效果会更好 |
20.现有含NaCl、Na2SO4和NaNO3的混合溶液,采用下列实验流程加入适当的试剂将其转化为相应的沉淀或固体,实现Cl-、SO42-和NO3-的相互分离:其中试剂1、2、4分别为( )
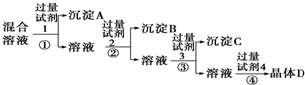

| A. | 硝酸银溶液 硝酸钡溶液 稀硝酸 | B. | 氯化钡溶液 稀硝酸 硝酸银溶液 | ||
| C. | 氢氧化钠溶液 硝酸银溶液 稀硝酸 | D. | 氯化钡溶液 硝酸银溶液 稀硝酸 |
7.下列说法中正确的是( )
| A. | 用到金属钠时,要用镊子取、再用小刀切下所需量,剩余的钠不能放回原试剂瓶中 | |
| B. | 大型中央空调的制冷剂可用液氨 | |
| C. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 | |
| D. | 测氯水的pH,可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较 |
4.工业制A1,你认为说法不妥当的是( )
| A. | 铝便于运输、贮存,从安全角度考虑,铝是最佳燃料之一 | |
| B. | 铝资源比较丰富,易于开采,且可以再生 | |
| C. | 铝燃烧热大,燃烧污染小,易有效控制 | |
| D. | 寻找高效催化剂,使A12O3分解同时释放能量,是铝能源大规模开发利用的一项关键技术 |
5.观察是研究物质性质一种基本方法.某同学将一小块金属钠露置空气中,观察到如下现象:银白色$\stackrel{①}{→}$变灰暗$\stackrel{②}{→}$变白色$\stackrel{③}{→}$出现液滴$\stackrel{④}{→}$白色固体,下列说法正确的是( )
| A. | ①是化合反应 | |
| B. | ②变白色是因为生成了碳酸钠 | |
| C. | ③是碳酸钠吸收空气中的水蒸气形成了溶液 | |
| D. | ④只发生物理变化 |

 .
.