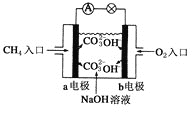
��Ŀ����
����Ŀ�����ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
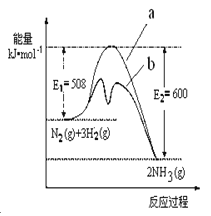
(1) ����ͼ�ṩ����Ϣ��д���÷�Ӧ���Ȼ�ѧ���� ����ͼ�������� ������a�� ����b������ʾ��������ý�������仯���ߡ�
(2) �ں�����������������������˵��������Ӧ�Ѵ�ƽ�����
A��3v(H2)��=2v(NH3)��
B����λʱ��������n mol N2��ͬʱ����2n molNH3
C��������������ܶȲ���ʱ��ı仯���仯
D��������ѹǿ����ʱ��ı仯���仯
���𰸡�(1)N2(g)+3H2(g)![]() 2NH3(g)��H=-92kJ/mol��b(2)BD
2NH3(g)��H=-92kJ/mol��b(2)BD
��������
�������������ͼ���������Ӧ����H=508-600=-92KJ/mol�� (1) N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92kJ/mol��(2) A��3v(H2)��=2v(NH3)�� ����֮�ȵ���ϵ������������B����λʱ��������n mol N2��ͬʱ����2n molNH3 ��B��ȷ��C����Ӧǰ����������������䣬������������䣬�ܶ��κ�ʱ��������������ܶȲ���ʱ��ı仯���仯�����ж��Ƿ�ƽ����D����Ӧǰ���������������ȣ�������ѹǿ����ʱ��ı仯���仯��D��ȷ��
2NH3(g) ��H=-92kJ/mol��(2) A��3v(H2)��=2v(NH3)�� ����֮�ȵ���ϵ������������B����λʱ��������n mol N2��ͬʱ����2n molNH3 ��B��ȷ��C����Ӧǰ����������������䣬������������䣬�ܶ��κ�ʱ��������������ܶȲ���ʱ��ı仯���仯�����ж��Ƿ�ƽ����D����Ӧǰ���������������ȣ�������ѹǿ����ʱ��ı仯���仯��D��ȷ��

����Ŀ������Ǧ(PbSO4)�㷺Ӧ��������Ǧ���ء���ɫ���ϵȡ����÷�Ǧ��( PbS)ֱ���Ʊ�����Ǧ��ĩ���������£�
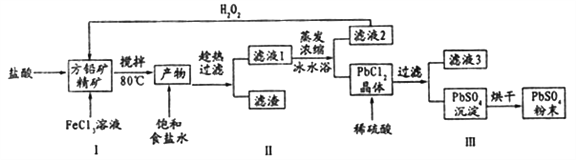
��֪��(i) PbCl2 (s)+2C1-(aq)=PbCl42-(aq) ��H>0
(ii)�й����ʵ�Ksp�ͳ���ʱ��pH���£�
���� | Ksp | ���� | ��ʼ����ʱpH | ��ȫ����ʱpH |
PbSO4 | 1.0��10-8 | Fe(OH)3 | 2.7 | 3.7 |
PbCl2 | 1.6��10-5 | Pb(OH)2 | 6 | 7.04 |
��1������I��Ӧ�����������Թ۲쵽����ɫ�������ɣ���д�������ӷ���ʽ___________��
��2���û�ѧƽ���ƶ���ԭ�����Ͳ������ʹ�ñ�ˮԡ��ԭ��____________��
��3�����������������п���ѭ�����õ�������______________��
��4��д���������PbCl2����ת��ΪPbSO4���������ӷ���ʽ________________��
��5��Ǧ��ұ�����ӹ���ʹˮ�����ؽ���Ǧ�ĺ����������������Ⱦ��ij�������Ʊ���һ��������Ǧ������EH��ʾ��������Чȥ��ˮ�еĺ���Ǧ����Ǧ��������Ҫ�����ķ�ӦΪ��2EH(s)+Pb2+![]() E2Pb(s)+2H+������Ǧ������ʵ�pH��ΧΪ____�����ţ�
E2Pb(s)+2H+������Ǧ������ʵ�pH��ΧΪ____�����ţ�
A.4��5 B.6��7 C.9��10 D.11��12
��6��PbSO4�ȼ����ؿ���������������Ĺ�����Դ�������ṹ��ͼ��ʾ��������Ϊ����ʵ���ˮLiCl-KC1������������ں�ؼ���˲��������ܡ��õ���ܷ�ӦΪPbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb��

�ٷŵ�����У�Li+��_______�ƶ����������������������
�ڸ�����ӦʽΪ_____________��
�۵�·��ÿת��0.2mol���ӣ�����������_________g Pb��