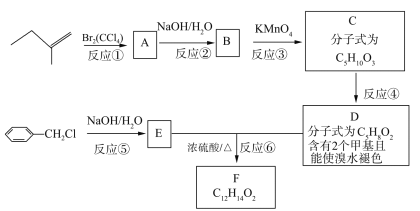
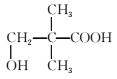
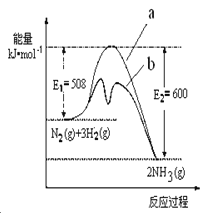
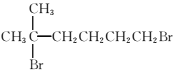题目内容
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空。
(1)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。负极反应式为________________________________;反应一段时间后负极的质量_________(填“增重”或“减少”或“不变”)
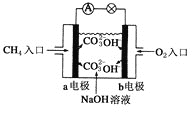
(2)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图,该电池极的负电极反应式是:________________________;标准状况下,2.24L的甲烷全部反应后,电子转移________ mol。
(3)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和插入烧碱溶液中(b组),都形成了原电池,在a组原电池中,负极材料为______;写出b组插入烧碱溶液中形成原电池的负极反应式:_________________________。
【答案】 Pb+SO42-–2e-=PbSO4 增重 CH4+10OH-–8e-=CO32—+7H2O 0.8 Cu Al+4OH-–3e-=AlO2-+2H2O
【解析】(1)根据总方程式可知负极是Pb失去电子转化为硫酸铅,反应式为Pb+SO42-–2e-=PbSO4,因此反应一段时间后负极的质量增重;(2)甲烷在负极通入,发生失去电子的氧化反应,电解质溶液显碱性,则该电池极的负电极反应式是CH4+10OH-–8e-=CO32—+7H2O;标准状况下,2.24L的甲烷是0.1mol,全部反应后,电子转移0.8mol。(3)常温下铝在浓硝酸中钝化,将铝片和铜片用导线相连,插入浓硝酸中铝是正极,铜是负极;铝能与氢氧化钠溶液反应,所以插入烧碱溶液中铝是负极,负极反应式为Al+4OH-–3e-=AlO2-+2H2O。

【题目】根据下列实验现象所得出的结论正确的是
选项 | 实验现象 | 实验结论 |
A | 将铝片分别投入浓、稀硝酸中,前者无明显现象,后者反应剧烈 | 稀硝酸的氧化性比浓硝酸的强 |
B | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色变浅 | Na2CO3溶液中存在水解平衡 |
C | 某溶液中滴加过量氨水产生白色沉淀且不溶解 | 该溶液中一定含有Mg2+ |
D | 溴水中通入SO2,溴水褪色 | SO2具有漂白性 |
A. A B. B C. C D. D