题目内容
【题目】一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g),反应过程如下图所示,下列说法正确的是
2NH3(g),反应过程如下图所示,下列说法正确的是
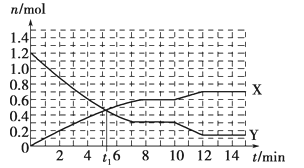
A. t1 min时正、逆反应速率相等
B. X曲线表示NH3的物质的量随时间变化的关系
C. 0~8 min,H2的平均反应速率v(H2)=3/4 mol·L-1·min-1
D. 10~12 min,N2的平均反应速率v(N2)=0.25 mol·L-1·min-1
【答案】B
【解析】
A、根据该图像可知平衡时X的物质的量增加0.6mol,Y的物质的量减少1.2mol-0.3mol=0.9mol,0.6:0.9=2:3,说明X是氨气,Y是氢气。t1 min时X与Y的物质的量相等,但未达平衡,所以正逆反应的速率不相等,A错误;
B、根据A的分析可知X是氨气,X曲线表示NH3的物质的量随时间变化的关系,B正确;
C、0~8 min,H2的平均反应速率v(H2)=0.9mol/(10L×8min)=0.01125 mol·L-1·min-1,C错误;
D、10~12 min,H2的平均反应速率为v(H2)=(0.3-0.15)mol/(10L×2min)=0.0075 mol·L-1·min-1,氮气的反应速率是氢气反应速率的1/3,则N2的平均反应速率为v(N2)=0.0075 mol·L-1·min-1/3=0.0025 mol·L-1·min-1,D错误;
答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目