题目内容
2C+O2=2CO; 2CO+O2═2CO2 都是放热反应,据此判断下列说法不正确的是(其它条件相同)( )A.12gC所具有的能量一定高于28gCO所具有的能量
B.28gCO和16O2所具有的总能量一定高于44gCO2所具有的总能量
C.12gC和32O2所具有的总能量一定高于44gCO2所具有的总能量
D.将一定质量的碳燃烧,生成CO2比生成CO时放出的热量多
【答案】分析:根据放热反应中反应物总能量大于生成物总能量来解答.
解答:解:A、因2C+O2=2CO是放热反应,所以12gC和16gO2所具有的能量一定高于28gCO所具有的能量,故A错误;
B、因2CO+O2═2CO2是放热反应,所以28gCO和16O2所具有的总能量一定高于44gCO2所具有的总能量,故B正确;
C、因2C+O2=2CO,2CO+O2═2CO2都是放热反应,则C+O2=CO2也是放热反应,所以12gC和32O2所具有的总能量一定高于44gCO2所具有的总能量,故C正确;
D、因物质完全燃烧放出的热量多,所以一定质量的碳燃烧,生成CO2比生成CO时放出的热量多,故D正确;
故选A.
点评:本题考查放热反应,解此类题要明确,反应物能量是指所有反应物的总能量,生成物能量是指所有生成物能量和,而不是某一个反应物和某一个生成物能量进行对比.
解答:解:A、因2C+O2=2CO是放热反应,所以12gC和16gO2所具有的能量一定高于28gCO所具有的能量,故A错误;
B、因2CO+O2═2CO2是放热反应,所以28gCO和16O2所具有的总能量一定高于44gCO2所具有的总能量,故B正确;
C、因2C+O2=2CO,2CO+O2═2CO2都是放热反应,则C+O2=CO2也是放热反应,所以12gC和32O2所具有的总能量一定高于44gCO2所具有的总能量,故C正确;
D、因物质完全燃烧放出的热量多,所以一定质量的碳燃烧,生成CO2比生成CO时放出的热量多,故D正确;
故选A.
点评:本题考查放热反应,解此类题要明确,反应物能量是指所有反应物的总能量,生成物能量是指所有生成物能量和,而不是某一个反应物和某一个生成物能量进行对比.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
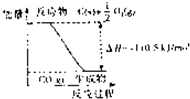 反应2C+O2=2CO的能量变化如图所示.下列说法正确的是( )
反应2C+O2=2CO的能量变化如图所示.下列说法正确的是( )| A、12 g C(s)与一定量O2(g)反应生成14 g CO(g),放出的热量为110.5 kJ | B、2 mol C(s)与足量02(g)反应生成CO2(g),放出的热量大于221 kJ | C、该反应的热化学方程式是:2C(s)+O2(g)=2CO(g);△H=-221kJ | D、碳的燃烧热为110.5kJ/mol |
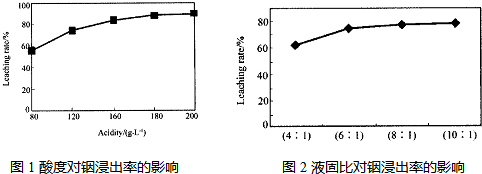

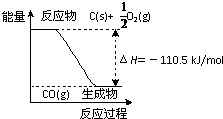 反应2C+O2=2CO 的能量变化如图所示.下列说法正确的是( )
反应2C+O2=2CO 的能量变化如图所示.下列说法正确的是( )