题目内容
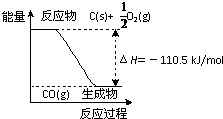 反应2C+O2=2CO 的能量变化如图所示.下列说法正确的是( )
反应2C+O2=2CO 的能量变化如图所示.下列说法正确的是( )分析:由图象可知,反应物总能量大于生成物总能量,反应放热,根据焓的差值可计算反应热,以此解答该题.
解答:解:A.反应生成14 g CO(g),应为0.5mol,放出的热量为
×110.5 kJ,故A错误;
B.反应热等于反应物的总键能与生成物总键能之差,故B错误;
C.反应热单位错误,应为kJ/mol,故C错误;
D.2 mol C(s)与足量O2(g)反应生成CO(g),放出的热量为221 kJ,CO继续燃烧放出热量,则反应生成CO2(g),放出的热量大于221 kJ,故D正确.
故选D.
| 1 |
| 2 |
B.反应热等于反应物的总键能与生成物总键能之差,故B错误;
C.反应热单位错误,应为kJ/mol,故C错误;
D.2 mol C(s)与足量O2(g)反应生成CO(g),放出的热量为221 kJ,CO继续燃烧放出热量,则反应生成CO2(g),放出的热量大于221 kJ,故D正确.
故选D.
点评:本题考查反应热与焓变,题目难道不大,注意根据图象反应物与生成物总能量的关系进行判断,把握反应热的意义.

练习册系列答案
相关题目
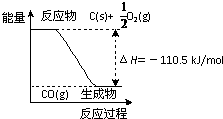 反应2C+O2=2CO 的能量变化如图所示.含11.2g KOH的稀溶液与1L0.1mol/L的H2SO4溶液反应放出11.46kJ的热量,下列说法正确的是( )
反应2C+O2=2CO 的能量变化如图所示.含11.2g KOH的稀溶液与1L0.1mol/L的H2SO4溶液反应放出11.46kJ的热量,下列说法正确的是( )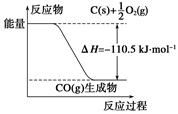
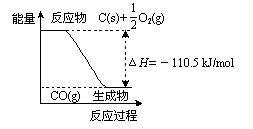 A.12 g C(s)与一定量O2(g)反应生成14 g CO(g),
A.12 g C(s)与一定量O2(g)反应生成14 g CO(g),