题目内容
(2012?南通模拟)某同学设计如下实验测量m g铜银合金样品中铜的质量分数:
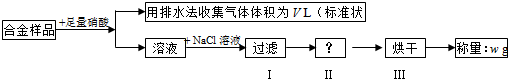
下列说法中不正确的是( )

下列说法中不正确的是( )
分析:A、由流程图可知,实验排水法收集,二氧化氮能与水反应生成NO,故不能金属与硝酸反应生成是NO或NO2或NO、NO2,最后收集的气体为NO;
B、过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒;
C、由流程图可知,溶液中加入氯化钠,将银离子转化为氯化银沉淀,通过测定氯化银沉淀的质量,计算银的质量,进而计算铜的含量,操作Ⅱ是在过滤之后,烘干之前,由于过滤后的氯化银附着一些离子,应洗涤附着的物质,防止影响氯化银的质量测定;
D、由流程图可知,实验原理为,在反应后溶液中加入氯化钠,将银离子转化为氯化银沉淀,通过测定氯化银沉淀的质量,计算银的质量,进而计算铜的含量.
B、过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒;
C、由流程图可知,溶液中加入氯化钠,将银离子转化为氯化银沉淀,通过测定氯化银沉淀的质量,计算银的质量,进而计算铜的含量,操作Ⅱ是在过滤之后,烘干之前,由于过滤后的氯化银附着一些离子,应洗涤附着的物质,防止影响氯化银的质量测定;
D、由流程图可知,实验原理为,在反应后溶液中加入氯化钠,将银离子转化为氯化银沉淀,通过测定氯化银沉淀的质量,计算银的质量,进而计算铜的含量.
解答:解:A、由流程图可知,实验排水法收集,二氧化氮能与水反应生成NO,故不能金属与硝酸反应生成是NO或NO2或NO、NO2,最后收集的气体为NO,故A错误;
B、过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒,故B正确;
C、由流程图可知,溶液中加入氯化钠,将银离子转化为氯化银沉淀,通过测定氯化银沉淀的质量,计算银的质量,进而计算铜的含量,操作Ⅱ是在过滤之后,烘干之前,由于过滤后的氯化银附着一些离子,应洗涤附着的物质,防止影响氯化银的质量测定,故操作Ⅱ应是洗涤,故C正确;
D、氯化银的质量为wg,所以合金中银的质量为
g,故合金中铜的质量分数为
×100%=
×100%,故D错误;
故选AD.
B、过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒,故B正确;
C、由流程图可知,溶液中加入氯化钠,将银离子转化为氯化银沉淀,通过测定氯化银沉淀的质量,计算银的质量,进而计算铜的含量,操作Ⅱ是在过滤之后,烘干之前,由于过滤后的氯化银附着一些离子,应洗涤附着的物质,防止影响氯化银的质量测定,故操作Ⅱ应是洗涤,故C正确;
D、氯化银的质量为wg,所以合金中银的质量为
| 108w |
| 143.5 |
m-
| ||
| m |
| 143.5m-108w |
| 143.5m |
故选AD.
点评:本题考查学生对实验原理的理解、物质组成的测定等,难度中等,理解原理是关键,需要学生具有扎实的基础知识与综合运用知识分析解决问题的能力.

练习册系列答案
相关题目
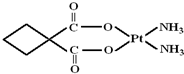 (2012?南通模拟)Ⅰ.顺铂是美国教授B Rosenberg等人于1969年发现的第一种具有抗癌活性的金属配合物,它的化学式为Pt(NH3)2Cl2.1995年WHO对上百种治癌药物进行排名,顺铂的综合评价列第2位.
(2012?南通模拟)Ⅰ.顺铂是美国教授B Rosenberg等人于1969年发现的第一种具有抗癌活性的金属配合物,它的化学式为Pt(NH3)2Cl2.1995年WHO对上百种治癌药物进行排名,顺铂的综合评价列第2位.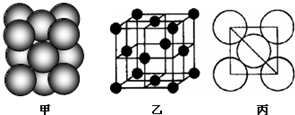
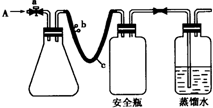 (2012?南通模拟)实验室用下列方法测定某水样中O2的含量.
(2012?南通模拟)实验室用下列方法测定某水样中O2的含量.