题目内容
9.下列一些生活中常见物质的相关说法正确的是( )| A. | 明矾和纯碱可分別用于水的消毒,洗涤油污 | |
| B. | 鸡蛋清溶液中加人饱和硫酸钠溶液•生成的沉淀物不能再溶解 | |
| C. | 紫色酸性离高锰酸钾溶液中加人植物油充分振荡后,溶液液分层且上层为紫色 | |
| D. | “84”消毒液溶液中滴加醋酸.KI淀粉溶液振荡后溶液变蓝色 |
分析 A、强氧化性的物质能够杀菌消毒,纯碱溶液去油污的原理,碳酸根离子的水解显碱性,油脂在碱溶液中发生水解生成溶于水的高级脂肪酸盐和甘油容易洗去,碳酸钠溶液中碳酸根离子水解是吸热反应,升温促进水解,溶液碱性增强,去污效果好;
B、蛋白质的盐析是可逆过程;
C、植物油中含有碳碳不饱和双键,能与高锰酸钾溶液反应;
D、次氯酸钠在酸溶液中可把KI氧化生成碘单质,淀粉遇碘变蓝色.
解答 解:A、有强氧化性的物质能够杀菌消毒,明矾不具有强的氧化性,不能杀菌消毒,用热的纯碱洗涤油污,是利用碳酸根离子水解呈碱性,酯类物质在碱性条件下水解生成高级脂肪酸钠和丙三醇,碳酸钠溶液中碳酸根离子水解是吸热反应,升温促进水解,溶液碱性增强,去污效果好,故A错误;
B、鸡蛋清溶液中加入饱和硫酸钠溶液发生盐析,盐析是可逆的,故B错误;
C、植物油中含有碳碳双键,能使酸性高锰酸钾紫色退去,故C错误;
D、“84”消毒液溶液中滴加醋酸,次氯酸钠在酸溶液中可把KI氧化生成碘单质,淀粉遇碘变蓝色,故D正确;
故选D.
点评 本题考查了物质性质的分析判断,蛋白质盐析现象,盐类水解原理应用氧化还原反应的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
10.在容积为2L密闭容器中,保持体系内温度800℃不变,将一定量的NO和O2混合发生反应:2NO+O2═2NO2,其中NO的物质的量[n(NO)]随时间的变化如表:
请回答问题:用O2表示达到平衡(假设30s刚刚达到平衡)时反应速率0.0011mol/(L.s),0~10s与10~20s的反应速率之比为5:1.
| 时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.2 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
17.按要求填空:
(1)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
①向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2═HCN+NaHCO3.
②不能证明HCN是弱电解质的方法是D
A.测得0.1mol/L HCN的pH>l
B.测得NaCN溶液的pH>7
C.0.1mol/L的HCN溶液与盐酸,稀释100倍后,HCN的pH大
D.用足量锌分别与相同浓度、相同体积的盐酸和HCN溶液反应,产生的氢气一样多
③25℃在CH3COOH与CH3COONa的溶液中,pH=6,则溶液中c(CH3COO-)/c(CH3COOH)=18.
(2)常温时,将某一元酸HA溶液与NaOH溶液等体积混合:
①若c (HA)=c (NaOH)=0.lmol/L,测得混合后溶液的pH>7.原因是(用离子方程式表示)A-+H2O?HA+OH-.
②若在100℃时,pH (HA)+(NaOH)=12,测得混合后溶液的显中性pH=6.当c(HA)=0.02mol/L,c(NaOH)═0.04mol/L时,将两种溶液等体积混合后,溶液中由水电离出的H+浓度为10-10mol/L,混合后溶液的pH=10(假设混合后溶液体积为两溶液体积之和).
(1)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②不能证明HCN是弱电解质的方法是D
A.测得0.1mol/L HCN的pH>l
B.测得NaCN溶液的pH>7
C.0.1mol/L的HCN溶液与盐酸,稀释100倍后,HCN的pH大
D.用足量锌分别与相同浓度、相同体积的盐酸和HCN溶液反应,产生的氢气一样多
③25℃在CH3COOH与CH3COONa的溶液中,pH=6,则溶液中c(CH3COO-)/c(CH3COOH)=18.
(2)常温时,将某一元酸HA溶液与NaOH溶液等体积混合:
①若c (HA)=c (NaOH)=0.lmol/L,测得混合后溶液的pH>7.原因是(用离子方程式表示)A-+H2O?HA+OH-.
②若在100℃时,pH (HA)+(NaOH)=12,测得混合后溶液的显中性pH=6.当c(HA)=0.02mol/L,c(NaOH)═0.04mol/L时,将两种溶液等体积混合后,溶液中由水电离出的H+浓度为10-10mol/L,混合后溶液的pH=10(假设混合后溶液体积为两溶液体积之和).
14.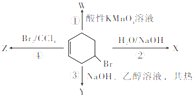 如图表示4-溴环己烯所发生的4个不同反应生成有机产物X、Y、Z、W,下列相关说法中不正确的是 ( )
如图表示4-溴环己烯所发生的4个不同反应生成有机产物X、Y、Z、W,下列相关说法中不正确的是 ( )
 如图表示4-溴环己烯所发生的4个不同反应生成有机产物X、Y、Z、W,下列相关说法中不正确的是 ( )
如图表示4-溴环己烯所发生的4个不同反应生成有机产物X、Y、Z、W,下列相关说法中不正确的是 ( )| A. | ①是氧化反应 | B. | Y、Z中均只含有一种官能团 | ||
| C. | Y是烃类丙可能有两种结构 | D. | X能与灼热的CuO反应生成醛类物质 |
1.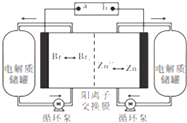 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )| A. | 充电时电极a连接电源的负极 | |
| B. | 放电时负极的电极反应式为2Br--2e-═Br2 | |
| C. | 放电时左侧电解质储罐中的离子总浓度增大 | |
| D. | 充电时右侧电极变粗.电解质溶液浓度減小 |
18.X、Y、Z都是气体,在减压或升温后,Z的物质的量都会增大的反应是( )
| A. | X+Y?3Z(正反应吸热) | B. | 2X+Y?2Z(正反应吸热) | ||
| C. | X+Y?2Z(正反应吸热) | D. | X+2Y?4Z(正反应放热) |
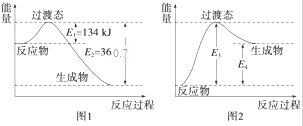
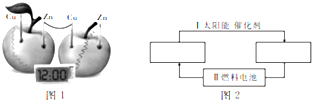 电化学知识可广泛应用于生产生活实际之中.
电化学知识可广泛应用于生产生活实际之中.