题目内容
6.如图是深海鱼油的结构键线式,回答: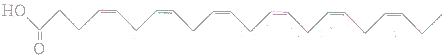
其中有22个碳原子,32个氢原子,2个氧原子,分子式是C22H32O2.
分析 键线式中拐点和端点表示C原子,每个C原子能形成四个共价键,根据键线式确定各元素原子个数及分子式.
解答 解:键线式中拐点和端点表示C原子,每个C原子能形成四个共价键,根据键线式知,C、H、O原子个数分别是22、32、2,分子式为C22H32O2,
故答案为:22;32;2;C22H32O2.
点评 本题考查键线式中分子式及原子个数判断,明确碳元素成键特点及键线式含义是解本题关键,注意每个C原子能形成四个共价键,不够四个共价键的用H原子补充,从而确定氢原子个数,题目难度不大.

练习册系列答案
相关题目
12.下表是第三周期部分主族元素的电离能数据:
下列说法不正确的是( )
| 元素 | I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 甲 | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
| 乙 | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
| 丙 | 786.5 | 1577.1 | 3231.6 | 4355.5 | 16091 |
| 丁 | 1251.2 | 2298 | 3822 | 5158.6 | 6542 |
| A. | 甲的金属性比乙强,且甲和乙的最高价氧化物的水化物可以相互反应 | |
| B. | 乙的最外层电子轨道表达式: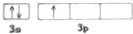 | |
| C. | 丙的最高价氧化物性质稳定,属于原子晶体,常温下不和强酸、强碱、强氧化剂反应 | |
| D. | 丁的常见的气态氢化物一定是极性分子 |
17.NA为阿伏加德罗常数,下列有关说法正确的是( )
| A. | 常温下,7.8 g 固体Na2O2中,含有的阴阳离子总数为0.4 NA | |
| B. | 4.48L氨气分子中含0.6NA个N-H键 | |
| C. | 铁、Cu片、稀硫酸组成的原电池,当金属铁质量减轻5.6 g时,流过外电路的电子为0.3 NA | |
| D. | 4℃时,20 g 2H216O中含有共用电子对数为2 NA |
1.往硫酸铝溶液中逐滴滴入氨水溶液至过量,可观察到的现象是( )
| A. | 有白色絮状沉淀产生,且不溶解 | B. | 先有白色絮状沉淀,后又溶解 | ||
| C. | 一直无明显现象 | D. | 先无现象,后有白色絮状沉淀 |
11.中草药陈皮中含有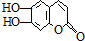 (碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )
(碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )
 (碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )
(碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用.1mol该物质与浓溴水作用和足量的NaOH溶液反应分别消耗的物质的量为( )| A. | 2moL,2moL | B. | 3 moL,3 moL | C. | 3 moL,4 moL | D. | 2 moL,4 moL |
18.化学与科学、技术、社会、环境密切相关,下列有关说法中正确的是( )
| A. | 医疗上广泛使用的酒精消毒剂是质量分数约为75%的乙醇溶液 | |
| B. | “西气东输”中的“气”指的是煤气 | |
| C. | 苯的产量可以衡量一个国家的石油化工发展水平 | |
| D. | 用浸泡过高锰酸钾溶液的硅土来吸收水果或者花朵产生的乙烯,以达到保鲜的要求 |
15.下列各项正确的是( )
| A. | .钠与水反应的离子方程式:Na+H2O═Na++OH-+H2↑ | |
| B. | 铁与水蒸气反应的化学方程式:2Fe+3H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe2O3+3H2 | |
| C. | .碳酸钠与少量盐酸反应的离子方程式:CO32-+H+═HCO3- | |
| D. | .钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+═2Na++Cu |
16.下列实验获得成功的是( )
| A. | 欲证明放入硫酸溶液中的纤维素加热已发生水解可向所得溶液中加入银氨溶液,放在水浴中 | |
| B. | 欲证明蔗糖的水解产物有葡萄糖,可向试管中加入0.5g蔗糖及质量分数为10%的稀硫酸4mL,加热3~4分钟,再向试管中加入新制Cu(OH)2煮沸,观察有红色沉淀生成 | |
| C. | 为证明硬脂酸有酸性,可以向滴有酚酞的稀NaOH溶液加入硬脂酸,并加热 | |
| D. | 用灼烧的方法检验是羊毛线还是蚕丝线 |
 .
.