题目内容
(8分) 关于反应热请回答如下问题:
(1)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为 。
(2) 实验测得,向200mL1mol/L的NaOH溶液中加入稀醋酸恰好反应放出Q kJ的热量,请写出热化学反应方程式:_________________________ 。
(3)已知反应CH3—CH3(g)―→CH2=CH2(g)+H2(g),有关化学键的键能如下。
试计算该反应的反应热___________________________
(4)利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列问题:已知:N2(g)+O2(g) = 2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g)+O2(g) = 2H2O(g) △H=-483.6kJ/mol
写出氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为 。
(1)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为 。
(2) 实验测得,向200mL1mol/L的NaOH溶液中加入稀醋酸恰好反应放出Q kJ的热量,请写出热化学反应方程式:_________________________ 。
(3)已知反应CH3—CH3(g)―→CH2=CH2(g)+H2(g),有关化学键的键能如下。
| 化学键 | C—H | C=C | C—C | H—H |
| 键能/kJ·mol-1 | 414.4 | 615.3 | 347.4 | 435.3 |
(4)利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列问题:已知:N2(g)+O2(g) = 2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol2H2(g)+O2(g) = 2H2O(g) △H=-483.6kJ/mol
写出氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为 。
(1)△H3>△H2>△H1;
(2) NaOH(aq)+CH3COOH(aq) CH3COONa(aq)+H2O(l)△H =-5QkJ/mol ;
CH3COONa(aq)+H2O(l)△H =-5QkJ/mol ;
(3) +125.6 kJ/mol;
(4)4 NH3(g) + 5O2(g) 4NO(g) + 6H2O(g);ΔH ="-" 905.5 kJ·mol-1。
4NO(g) + 6H2O(g);ΔH ="-" 905.5 kJ·mol-1。
(2) NaOH(aq)+CH3COOH(aq)
 CH3COONa(aq)+H2O(l)△H =-5QkJ/mol ;
CH3COONa(aq)+H2O(l)△H =-5QkJ/mol ;(3) +125.6 kJ/mol;
(4)4 NH3(g) + 5O2(g)
 4NO(g) + 6H2O(g);ΔH ="-" 905.5 kJ·mol-1。
4NO(g) + 6H2O(g);ΔH ="-" 905.5 kJ·mol-1。试题分析:(1)浓硫酸溶于水放热,醋酸为弱电解质,反应过程中醋酸发生电离,电离吸热,反应热为负值,放出的热量越多,则△H越小,则△H3>△H2>△H1;(2) 实验测得,向200mL1mol/L的NaOH溶液中加入稀醋酸恰好反应放出Q kJ的热量,热化学反应方程式:NaOH(aq)+CH3COOH(aq)
 CH3COONa(aq)+H2O(l)△H =-5QkJ/mol;(3)根据反应热等于反应物的键能之和减去生成物的键能之和进行计算。该反应的反应热=(6×414.4+347.4)-(4×414.4+615.3+435.3)="+125.6" kJ/mol;(4)①N2(g)+O2(g) = 2NO(g) △H=+180.5kJ/mol;②N2(g)+3H2(g)
CH3COONa(aq)+H2O(l)△H =-5QkJ/mol;(3)根据反应热等于反应物的键能之和减去生成物的键能之和进行计算。该反应的反应热=(6×414.4+347.4)-(4×414.4+615.3+435.3)="+125.6" kJ/mol;(4)①N2(g)+O2(g) = 2NO(g) △H=+180.5kJ/mol;②N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ/mol③2H2(g)+O2(g) = 2H2O(g) △H=-483.6kJ/mol。根据盖斯定律:①×2+③×3-②×2得氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为4 NH3(g) + 5O2(g)
2NH3(g) △H=-92.4kJ/mol③2H2(g)+O2(g) = 2H2O(g) △H=-483.6kJ/mol。根据盖斯定律:①×2+③×3-②×2得氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为4 NH3(g) + 5O2(g) 4NO(g) + 6H2O(g);ΔH ="-" 905.5 kJ·mol-1。
4NO(g) + 6H2O(g);ΔH ="-" 905.5 kJ·mol-1。
练习册系列答案
相关题目
 N2↑+ 4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
N2↑+ 4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
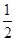 Cl2(g)===NaCl(s) ΔH1
Cl2(g)===NaCl(s) ΔH1