题目内容
【题目】Ⅰ.国产C919大型客机的正式下线,标志着我国航空工业进入了新的发展阶段,我国成为世界上少数几个具有自行研制大型飞机的国家之一。
(1)飞机的外壳通常采用镁一铝合金材料,铝的价电子排布图为_______________,第一电离能:铝________(填“大于”或“小于”)镁。
(2)为了减轻质量而不减轻外壳承压能力,现代飞机通常采用复合材料一玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51型环氧树脂中部分结构如图甲所示,其中碳原子的杂化方式为___________,该材料此部分中所含元素的电负性从小到大的顺序为_______________。

II.大型飞机的发动机在制造过程中通常采用碳化钨做关键部位的材料。
(1)钨元素位于周期表的第六周期第VIB族,请写出其位于同一族的元素铬的原子的价电子排布式__________________,
(2)图乙为碳化钨晶体的一部分结构,碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有_______个,1个钨原子周围距离钨原子最近的碳原子有_______个,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是___________(填序号)。
A.Fe Cu B.Ti Au C.Mg Zn D.Cu Ag
(4)设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏加德罗常数NA用上述数据可以表示为____________________。
【答案】 ![]() 小于 sp2、sp3杂化 H<C<O 3d54s1 6 6 B
小于 sp2、sp3杂化 H<C<O 3d54s1 6 6 B ![]()
【解析】本题主要考查物质结构。
Ⅰ.(1)飞机的外壳通常采用镁一铝合金材料,铝的价电子排布图为![]() ,镁的3p电子半充满,能量低,较稳定,所以第一电离能:铝小于镁。
,镁的3p电子半充满,能量低,较稳定,所以第一电离能:铝小于镁。
(2)常见的E51型环氧树脂中部分结构如图24 甲所示,其中单键碳原子的杂化方式为sp3杂化,双键碳原子的杂化方式为sp2杂化,该材料此部分中所含元素的电负性从小到大的顺序为H<C<O。
II.(1)元素铬的原子的价电子排布式:3d54s1。
(2)在此结构中,其中钨原子有6个,1个钨原子周围距离钨原子最近的碳原子有6个,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是B。
(4)该部分晶体含有6个碳原子,6个钨原子,b=6M/(VNA),NA=![]() 。
。

【题目】人们常常利用化学反应中的能量变化为人类服务。
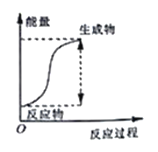
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大最的热。氢气燃烧生成水蒸气的能最变化如下图所示:

根据上图可知,在化学反应中,不仅存在物质的变化,而且伴随着______变化,1molH2完全燃烧生成1molH2O(气态)时,释放的能量是_______kJ。
(2)下列化学反应在理论上可以设计成原电池的是________。
A.Fe+2FeCl3=3FeCl2 B.SO3+H2O=H2SO4
C.CH4+2O2![]() CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
(3)下图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下:

a.电流计指针偏转 |
b.Cu极有H2产生 |
c.H+向负极移动 |
d.电流由Zn经导线流向Cu |
①实验报告中记录合理的是_______(填序号)。
②请写出该电池的负极反应式_________。
③若有1mol电子流过导线,则理论上产生H2的质量为______g.
④将稀H2SO4换成CuSO4溶液,电极质量增加的是______(填“锌极”或“铜极”,下同),溶液中SO42-移向_______。