题目内容
现有一Na2SO3、Na2SO4混合物样品ag,为了测定其中Na2SO3的质量分数,设计了如下方案,其中明显不合理的是
| A.将样品配制成溶液V1L,取其中25.00mL用标准KMnO4溶液滴定,消耗标准KMnO4溶液V2mL |
| B.向样品中加足量H2O2,再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg |
| C.将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为cg |
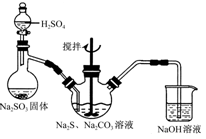
| D.将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHSO3的洗气瓶、盛有浓H2SO4的洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重dg |
D
试题分析:D中想通过测生成的SO2的质量得亚硫酸钠,从而得出其质量分数,但不能保证生成的二氧化硫全部被碱石灰吸收,有部分二氧化硫留在装置中,故测得结果不准确,D项不合理;故选D;A、Na2SO3与高锰酸钾发生氧化还原,通过高锰酸钾的量求出亚硫酸钠的量,从而求得亚硫酸钠的质量分数,故A正确;B、H2O2把亚硫酸钠氧化成硫酸钠,加入足量BaCl2溶液把硫酸根全部转化成沉淀,通过测沉淀的质量得出硫酸钡的物质的量,根据原子守恒,硫酸钡的物质的量等于亚硫酸钠和硫酸钠的物质的量之和,根据两者总物质的量和总质量可求得亚硫酸钠的质量分数;C、盐酸把亚硫酸钠反应掉,氯化钡与硫酸钠反应转化成硫酸钡沉淀,求出硫酸钠的量,再求出亚硫酸钠,故C正确;故选D。

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
 CO2(g) ?H=-283.0 kJ/mol
CO2(g) ?H=-283.0 kJ/mol