题目内容
【题目】甲醇是一种重要的有机原料,在催化剂的作用下,CO和H2反应可生成甲醇 (CH3OH) 和副产物CH4,反应如下:
反应①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.0kJ/mol
CH3OH(g) △H1=-90.0kJ/mol
反 应②CO(g)+3H2(g)![]() CH4(g) + H2O(g) △H2
CH4(g) + H2O(g) △H2
反应③ CH4(g)+2H2O(g)![]() CO2(g)+ 4H2(g) △H3=+125.0 kJ/mol
CO2(g)+ 4H2(g) △H3=+125.0 kJ/mol
反应④CO(g)+ H2O(g)![]() CO2(g) + H2(g) △H4=-25.0 kJ /mol
CO2(g) + H2(g) △H4=-25.0 kJ /mol
K1、K2、K3、K4分别表示反应①、②、③、④的平衡常数。
回答下列问题:
(1)反应②的平衡常数的表达式为K2=______________,K2与K3和K4的关系为K2=______________,△H2=____________kJ/mol。
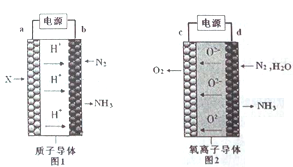
(2)图1中能正确表示反应①的平衡常数(lgK1) 随温度变化的曲线为______________(填曲线字母),其判断理由为______________________________________________________________。

(3)恒温恒容的条件下,下列情况能说明反应①达到平衡状态的是__________________。
A.2v正 (H2)=v逆(CH3OH) B.混合气体的密度不再改变
C.混合气体的平均摩尔质量不再改变 D.混合气体的压强不再改变
(4)为探究不同催化剂对CO和H2生成CH3OH的选择性效果,某实验室控制CO和H2的初始投料比为1∶3进行实验,得到如下数据:
T/K | 时间/min | 催化剂种类 | 甲醇的含量(%) |
450 | 10 | CuO-ZnO | 78 |
450 | 10 | CuO-ZnO-ZrO2 | 88 |
450 | 10 | ZnO-ZrO2 | 46 |

①由表1可知,反应①的最佳催化剂为______________,图2中a、b、c、d四点是该温度下CO平衡转化率的是_________________________________。
②有利于提高CO转化为CH3OH的平衡转化率的措施有_________________。
A.使用催化剂CuO-ZnO-ZrO2 B.适当降低反应温度
C.增大CO和H2的初始投料比 D.恒容下,再充入a molCO和3a mol H2
(5)已知1000℃,反应CO(g)+ H2O(g)![]() CO2(g) + H2(g) K4=1.0。该温度下,在某时刻体系中CO、H2O、CO2、H2的浓度分别为3molL-1、1molL-1、4molL-1、2molL-1,则此时上述反应的v正(CO)_______v逆(CO) (填“>”、“<”或“=”)达到平衡时c(CO)=___________ molL-1。
CO2(g) + H2(g) K4=1.0。该温度下,在某时刻体系中CO、H2O、CO2、H2的浓度分别为3molL-1、1molL-1、4molL-1、2molL-1,则此时上述反应的v正(CO)_______v逆(CO) (填“>”、“<”或“=”)达到平衡时c(CO)=___________ molL-1。
【答案】 c(CH4)c(H2O)/[ c(CO)c3 (H2)] K4/K3 -150.0 A 该反应为放热反应,升高温度,平衡逆向移动,K减小,lgK减小 CD CuO-ZnO-ZrO2 cd BD < 3.5
【解析】(1)反应②的平衡常数的表达式为K2= c(CH4)c(H2O)/[ c(CO)c3 (H2)];反应②=反应④-反应③,所以K2= K4/K3;△H2=△H4-△H3=-25.0kJ/mol-(+125.0kJ/mol)= -150.0 kJ/mol。
(2)反应①正反应为放热反应,温度升高,平衡逆向移动,平衡常数K减小,lgK减小,故能正确表示反应①的平衡常数(lgK1)随温度变化的曲线为A。答案为:A、该反应为放热反应,升高温度,平衡逆向移动,K减小,lgK减小。
(3)A、当v正(H2)= 2v逆(CH3OH),可以说明反应已达平衡,A中速率的比值关系搞错,A不可以说明;B、恒温恒容下,混合气体的密度始终不改变,B不可以说明;C、混合气体的总质量不变,混合气体的物质的量随平衡的移动改变,故当混合气体的平均摩尔质量不再改变时,说明反应已达平衡,C可以说明;D、该反应是前后气体分子数发生改变的反应,当混合气体的压强不再改变时,说明反应已达平衡,D可以说明。故能说明反应①达到平衡状态的是CD。
(4)①由表1可知,温度相同时相同时间内,催化剂为CuO-ZnO-ZrO2时,甲醇的含量最高,所以反应①最好的催化剂为CuO-ZnO-ZrO2;反应①为放热反应,升高温度平衡逆向移动,K减小,图2中a到c段,K在增大,所以a到c段表示的是反应还未达到平衡,cd段才是平衡状态,即a、b点不是平衡点, c、d两点是相应温度下CO平衡转化率的点。 ②要提高CO转化为CH3OH的平衡转化率,对A:催化剂不影响平衡的移动,A错误;对B:该反应正反应为放热反应,适当降低温度,平衡右移,可以加大CO的转化率,B正确;对C:增大CO和H2的初始投料比,CO的转化率降低,C错误;对D:恒容下,再充入amolCO和3amolH2,先将这部分气体充入另一个容器,构成等效平衡,然后再压入原来容器,相当于增压,平衡右移,CO的转化率增大,D正确。故能提高CO转化率的是BD。
(5)某时刻该反应的浓度商Qc= c(CO2)c(H2)/[ c(CO)c(H2O)]=(4×2)/(3×1)=8/3> K4=1.0,所以反应在逆向进行,v正(CO)<v逆(CO);设平衡左移过程中再生成xmol /L的CO,则达平衡时,CO、H2O、CO2、H2的浓度分别为(3+x)molL-1、(1+x)molL-1、(4-x)molL-1、(2-x)molL-1,达平衡时有(2-x)×(4-x)/ [(3+x)×(1+x)]=1,解得x=0.5,所以平衡时CO的浓度为c=(3+0.5)molL-1=3.5mol/L。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】二甲醚(CH3OCH3)被称为21世纪的新型燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
化学反应方程式 | 化学平衡常数 | |
①CO(g)+2H2(g) | ΔH1=-99 kJmol-1 | K1 |
②2CH3OH(g) | ΔH2=-24 kJmol-1 | K2 |
③CO(g)+H2O(g) | ΔH3=-41 kJmol-1 | K3 |
(1)该工艺的总反应为3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g) ΔH
CH3OCH3(g)+CO2(g) ΔH
该反应ΔH=__________________,化学平衡常数K=____________________(用含K1、K2、K3的代数式表示)。
(2)某温度下,将8.0molH2和4.0molCO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g) ![]() CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则CO的转化率为________。
CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则CO的转化率为________。
(3)下列措施中,能提高CH3OCH3产率的有________。
A.分离出二甲醚 B.升高温度 C.改用高效催化剂 D.增大压强
(4)该工艺中反应③的发生提高了CH3OCH3的产率,原因是_______________________________。
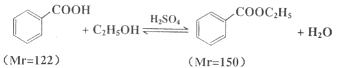
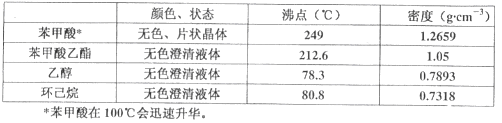
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
A.用CCl4提取溴水中的Br2[来 | B.从KI和I2的固体混合物中回收I2 | C.吸收NH3(极易溶于水),并防止倒吸 | D.工业酒精制备无水酒精 |
|
|
|
|
A. A B. B C. C D. D