题目内容
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
A.用CCl4提取溴水中的Br2[来 | B.从KI和I2的固体混合物中回收I2 | C.吸收NH3(极易溶于水),并防止倒吸 | D.工业酒精制备无水酒精 |
|
|
|
|
A. A B. B C. C D. D
【答案】A
【解析】
试题A.萃取剂的选择必须符合下列条件:溶质在萃取剂中的溶解度比在原溶剂中要大;萃取剂与原溶剂不相溶;萃取剂与溶质不反应,溴单质易溶于四氯化碳,且四氯化碳与水互不相溶,A正确;碘单质易升华,加热后,碘单质易升华,剩余的是KI,B错误;氨气极易溶于水而难溶于苯,该装置导管口插入水中,无法防止倒吸,C错误;该装置酒精灯的水银球应该在蒸馏烧瓶支管口处,冷却装置应该下口进水,上口出水,D错误。

 名校课堂系列答案
名校课堂系列答案【题目】甲醇是一种重要的有机原料,在催化剂的作用下,CO和H2反应可生成甲醇 (CH3OH) 和副产物CH4,反应如下:
反应①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.0kJ/mol
CH3OH(g) △H1=-90.0kJ/mol
反 应②CO(g)+3H2(g)![]() CH4(g) + H2O(g) △H2
CH4(g) + H2O(g) △H2
反应③ CH4(g)+2H2O(g)![]() CO2(g)+ 4H2(g) △H3=+125.0 kJ/mol
CO2(g)+ 4H2(g) △H3=+125.0 kJ/mol
反应④CO(g)+ H2O(g)![]() CO2(g) + H2(g) △H4=-25.0 kJ /mol
CO2(g) + H2(g) △H4=-25.0 kJ /mol
K1、K2、K3、K4分别表示反应①、②、③、④的平衡常数。
回答下列问题:
(1)反应②的平衡常数的表达式为K2=______________,K2与K3和K4的关系为K2=______________,△H2=____________kJ/mol。
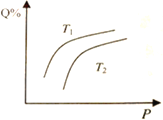
(2)图1中能正确表示反应①的平衡常数(lgK1) 随温度变化的曲线为______________(填曲线字母),其判断理由为______________________________________________________________。

(3)恒温恒容的条件下,下列情况能说明反应①达到平衡状态的是__________________。
A.2v正 (H2)=v逆(CH3OH) B.混合气体的密度不再改变
C.混合气体的平均摩尔质量不再改变 D.混合气体的压强不再改变
(4)为探究不同催化剂对CO和H2生成CH3OH的选择性效果,某实验室控制CO和H2的初始投料比为1∶3进行实验,得到如下数据:
T/K | 时间/min | 催化剂种类 | 甲醇的含量(%) |
450 | 10 | CuO-ZnO | 78 |
450 | 10 | CuO-ZnO-ZrO2 | 88 |
450 | 10 | ZnO-ZrO2 | 46 |

①由表1可知,反应①的最佳催化剂为______________,图2中a、b、c、d四点是该温度下CO平衡转化率的是_________________________________。
②有利于提高CO转化为CH3OH的平衡转化率的措施有_________________。
A.使用催化剂CuO-ZnO-ZrO2 B.适当降低反应温度
C.增大CO和H2的初始投料比 D.恒容下,再充入a molCO和3a mol H2
(5)已知1000℃,反应CO(g)+ H2O(g)![]() CO2(g) + H2(g) K4=1.0。该温度下,在某时刻体系中CO、H2O、CO2、H2的浓度分别为3molL-1、1molL-1、4molL-1、2molL-1,则此时上述反应的v正(CO)_______v逆(CO) (填“>”、“<”或“=”)达到平衡时c(CO)=___________ molL-1。
CO2(g) + H2(g) K4=1.0。该温度下,在某时刻体系中CO、H2O、CO2、H2的浓度分别为3molL-1、1molL-1、4molL-1、2molL-1,则此时上述反应的v正(CO)_______v逆(CO) (填“>”、“<”或“=”)达到平衡时c(CO)=___________ molL-1。