题目内容
在一个固定容积的密闭容器中,保持一定的温度进行以下反应:
A(g)+3B(g) 3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.
3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.
(1)达到平衡时C在反应混合体中体积百分含量是
×100%
×100%(用含a的关系式表示)
(2)在相同的实验条件下,若在同一个容器中改为加入2molA和6molB,达到平衡后,C在混合气体中的体积百分含量
(3)若在同一个容器中改为加入2molA和6molB,能否通过调节C的物质的量,使平衡时C在混合气体中的百分含量与原平衡相同?
(4)在相同的实验条件下,如果加入n mol A、m mol B和p molC,若要求平衡后C在混合气体中的百分含量保持不变,与(1)相同,则n、m与p的关系式为
A(g)+3B(g)
 3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.
3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.(1)达到平衡时C在反应混合体中体积百分含量是
| (3-3a) |
| (3+a) |
| (3-3a) |
| (3+a) |
(2)在相同的实验条件下,若在同一个容器中改为加入2molA和6molB,达到平衡后,C在混合气体中的体积百分含量
增大
增大
(填“增大”“减小”或“不变”).(3)若在同一个容器中改为加入2molA和6molB,能否通过调节C的物质的量,使平衡时C在混合气体中的百分含量与原平衡相同?
能,移走3molC.
能,移走3molC.
(如果能,请写出C的物质的量,如不能,请说明通过什么方法可以实现.)(4)在相同的实验条件下,如果加入n mol A、m mol B和p molC,若要求平衡后C在混合气体中的百分含量保持不变,与(1)相同,则n、m与p的关系式为
n+
=1,m+p=31,m=3n
| p |
| 3 |
n+
=1,m+p=31,m=3n
.| p |
| 3 |
分析:(1)根据差量法计算出混合气体物质的量的变化、C的物质的量,进而求出平衡时混合气体的总物质的量,再根据体积百分含量的定义计算;
(2)恒温恒容下,开始加入2molA和6molB,可等效为原平衡压强增大一倍,平衡向体积减小方向移动;
(4)恒温恒容情况下,对于前后气体体积变化的反应,构成等效平衡,按化学计量数转化到一边满足对应物质的物质的量相等即可.
(2)恒温恒容下,开始加入2molA和6molB,可等效为原平衡压强增大一倍,平衡向体积减小方向移动;
(4)恒温恒容情况下,对于前后气体体积变化的反应,构成等效平衡,按化学计量数转化到一边满足对应物质的物质的量相等即可.
解答:解:(1)A(g)+3B(g) 3C(g) 物质的量减少△n
3C(g) 物质的量减少△n
1mol 3mol 1mol
(1-a)mol 3(1-a)mol (1-a)mol
所以平衡时混合气体的总物质的量为1mol+3mol-(1-a)mol=(3+a)mol,
平衡时C在反应混合体中体积百分含量为
×100%=
×100%,
故答案为:
×100%;
(2)恒温恒容下,开始加入2molA和6molB,可等效为原平衡压强增大一倍,增大压强平衡向气体体积减小的方向移动,即向正反应移动,C在混合气体中的体积百分含量增大,
故答案为:增大;
(3)恒温恒容下,开始加入2molA和6molB,由(2)可知,平衡时C在混合气体中的体积百分含量比原平衡大,若再加入C,平衡向逆反应移动,平衡时C的含量比原平衡更高.若移走C平衡向正反应移动,可以降低C的含量,当移走得3molC相当于开始加入1molA和3molB,则达到的平衡时C在混合气体中的体积百分含量比原平衡相同,所以能通过调节C的物质的量,需移走3molC,故答案为:能,移走3molC;
(4)恒温恒容情况下,对于前后气体体积变化的反应,构成等效平衡,按化学计量数转化到左边满足1molA和3molB即可,所以有:n+
=1; m+p=31;整理得m=3n
故答案为:n+
=1,m+p=31,m=3n.
 3C(g) 物质的量减少△n
3C(g) 物质的量减少△n1mol 3mol 1mol
(1-a)mol 3(1-a)mol (1-a)mol
所以平衡时混合气体的总物质的量为1mol+3mol-(1-a)mol=(3+a)mol,
平衡时C在反应混合体中体积百分含量为
| 3(1-a)mol |
| (3+a)mol |
| (3-3a) |
| (3+a) |
故答案为:
| (3-3a) |
| (3+a) |
(2)恒温恒容下,开始加入2molA和6molB,可等效为原平衡压强增大一倍,增大压强平衡向气体体积减小的方向移动,即向正反应移动,C在混合气体中的体积百分含量增大,
故答案为:增大;
(3)恒温恒容下,开始加入2molA和6molB,由(2)可知,平衡时C在混合气体中的体积百分含量比原平衡大,若再加入C,平衡向逆反应移动,平衡时C的含量比原平衡更高.若移走C平衡向正反应移动,可以降低C的含量,当移走得3molC相当于开始加入1molA和3molB,则达到的平衡时C在混合气体中的体积百分含量比原平衡相同,所以能通过调节C的物质的量,需移走3molC,故答案为:能,移走3molC;
(4)恒温恒容情况下,对于前后气体体积变化的反应,构成等效平衡,按化学计量数转化到左边满足1molA和3molB即可,所以有:n+
| p |
| 3 |
故答案为:n+
| p |
| 3 |
点评:本题考查化学平衡移动与计算、等效平衡等,难度中等,注意等效思想的运用与理解.

练习册系列答案
相关题目
在一个固定容积的密闭容器中,可发生以下反应:A(g)+B(g)?xC(g);△H=?符合下图(a)所示的关系,由此推断关于图(b)的说法正确的是( )
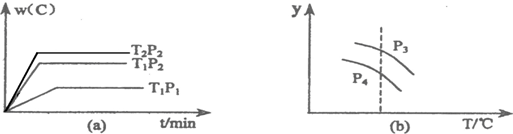

| A、P3>P4,y轴表示A的转化率 | B、P3<P4,y轴表示B的体积分数 | C、P3>P4,y轴表示混合气体的平均相对分子质量 | D、P3>P4,y轴表示混合气体的密度 |
在一个固定容积的密闭容器中,加入m mol A、n mol B,发生下列反应:mA(g)+nB(g)?pC(g),平衡时C的浓度是w mol/L,若容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,若要平衡后C的浓度仍为w mol/L,则a、b、c应满足的关系是( )
| A、a:b:c=m:n:p | ||||||
B、a:b=m:n,
| ||||||
C、
| ||||||
D、a=
|
 2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为p mol/L,且C的体积分数为ω.在相同条件下:
2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为p mol/L,且C的体积分数为ω.在相同条件下: 2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中.
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中. 化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.