题目内容
根据下图回答问题: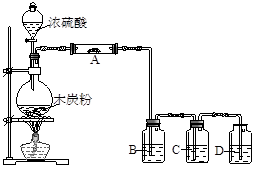
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,观察不到明显的现象,可以用一种简单的方法证明该装置不漏气,其方法和现象是 证明该装置不漏气。
(2)烧瓶中发生反应的化学方程式为: 。
(3)欲用图中的装置检验上述反应的全部产物。①仪器A要检验产物中的水,则A中的固体是 ;②B中装入品红溶液,目的是检验 ;③D中装入澄清石灰水以检验产物中的CO2,要使其它气体不干扰D中CO2的检验,则C中应装入的溶液是 。
(1)(3分)点燃酒精灯微热烧瓶一会儿(1分),在瓶B、C、D中出现气泡(1分),熄灭酒精灯冷却至室温(或冷却后),瓶B、C、D中导管液面上升并形成稳定的液柱,(1分)。
[或用止水夹夹住C与D间的橡胶管(1分),在分液漏斗中加水,如果水流了一部分后不再流下(1分)]
(2)(2分)2H2SO4(浓)+C CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(3)(3分)①无水硫酸铜(1分) ②SO2(1分) ③酸性KMnO4溶液(或溴水,1分)
解析试题分析:检查装置的气密性可以点燃酒精灯微热烧瓶一会,若在瓶B、C、D中出现气泡,熄灭酒精灯冷却至室温(或冷却后),瓶B、C、D中导管液面上升并形成稳定的液柱,则说明该装置的气密性是良好的。浓硫酸具有强氧化性,因此可以跟木炭反应生成二氧化碳、二氧化硫和水。一般用无水硫酸铜来检验水。二氧化硫能使品红溶液褪色。二氧化碳和二氧化硫都能使澄清石灰水变浑浊,因此为排除二氧化硫的干扰应用高锰酸钾溶液除掉二氧化硫。
考点:考查浓硫酸性质的相关知识点。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案碳及其化合物有广泛的用途。
(1)在电化学中,常用碳作电极:
①在酸性锌锰干电池中,碳棒作 极。
②若用碳棒和铁棒做电极电解饱和食盐水生产烧碱时,碳棒作 极,反应的离子方程式 。
(2)将水蒸气通过红热的碳可产生水煤气:C(s)+H2O(g)  CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。
CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。
| A.升高温度 | B.增加碳的用量 |
| C.加入催化剂 | D.用CO吸收剂除去CO |
 CO2(g)+H2(g)得到如下数据:
CO2(g)+H2(g)得到如下数据:| 温度/℃ | 起始浓度mol/L | 平衡浓度mol/L | |
| CO(g) | H2O(g) | H2(g) | |
| 900 | 2.0 | 0.8 | 0.4 |
通过计算,该反应的平衡常数为: 。
(4)工业上把水煤气中的混合气体处理后,获得较纯的H2用于合成氨:
N2(g)+3H2(g)一定条件下2NH3(g) △H= —92.4kJ/mol某同学在不同实验条件下模拟化工生产进行实验,N2浓度随时间变化如图:
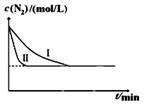
①与实验I比较,实验II改变的条件为: 。
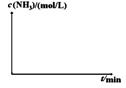
②实验III比实验I的温度要高,其它条件相同,请在下图画出实验I和实验III中NH3浓度随时间变化的示意图。
(18分) (1)某实验小组的甲同学用图l所示装置制取少量乙酸乙酯(加热设备及夹持固定装置均略去)。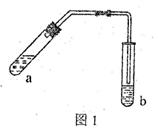

①试管a中需要加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序及操作是 。
②试管a中加入碎瓷片的作用是 ,如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是 (填序号)。
| A.立即补加 | B.不需补加 | C.冷却后补加 | D.重新配料 |
④试管b中盛有饱和Na2CO3溶液,其作用是 。
⑤反应结束后,振荡试管b,静置。观察到的现象是 。
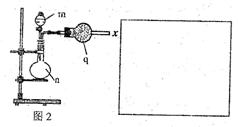
(2)该小组的乙同学利用图2所示装置制备并收集干燥的NO2气体。
①图2中仪器n的名称是 。
②请在方框内画出用集气瓶收集NO2的装置图。
③写出仪器n中发生反应的离子方程式: 。
(3)该小组的丙同学利用图2所示装置制取NH3和O2的混合气体,并且利用图3所示装置验证NH3的某些性质。m中加入浓氨水,q中加入碱石灰,e内放置催化剂(铂石棉),按气流方向连接各仪器x→y→z→h。
①图2仪器n内需加入固体试剂的名称为 。
②实验中观察到e内有红棕色气体出现,证明氨气具有 性,e中发生反应的化学方程式为 。