题目内容
亚氯酸钠(NaC1O2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖,油脂的漂白与杀菌.以下是过氧化氢法生产亚氯酸钠的工艺流程图: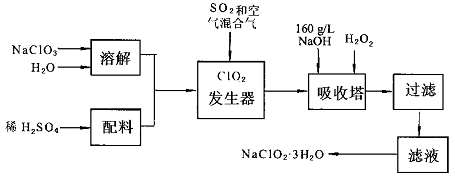
已知:①NaC1O2的溶解度随温度升高而增大,适当条件下可结晶析出NaC1O2·3H2O.
②纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全.
I.请根据上述流程回答下列问题
(1)发生器中鼓入空气的作用可能是
(2)吸收塔内的反应的化学方程式为 .吸收塔的温度不能超过20℃,其目的是 .
(3)在碱性溶液中NaC1O2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 .
(4)从滤液中得到NaC1O2·3H2O粗晶体的实验操作依次是 .
II.上述流程中的原料NaC1O3可由氯气通入热的烧碱溶液后重结晶就得到比较纯净的产品,所以通常工厂联合氯碱车间制备.
(1)氯碱工业中的原料为 ,原料需要净化的原因是 ,阳极产品为
(2)工业生产NaC1O3的化学方程式为
Ⅰ(1)稀释C1O2以防止爆炸;(2)2NaOH+2C1O2+H2O2=2NaC1O2+2H2O+O2 防止H2O2分解
(3)连续测定吸收塔内溶液的pH; (4)蒸发,冷却结晶,过滤
Ⅱ.(1)饱和食盐水 防止堵塞离子交换膜 氯气 (2)3Cl2+6NaOH==5NaCl+NaClO3+3H2O
解析试题分析:(1)发生反应产生的C1O2不稳定易分解爆炸。鼓入空气的作用把它稀释至0%以下安全含量。(2)吸收塔内的反应的化学方程式为:2NaOH+2C1O2+H2O2=2NaC1O2+2H2O+O2。过氧化氢不稳定,高温容易分解。吸收塔的温度不能超过20℃,其目的是防止H2O2分解。(3)判断NaOH是否过量的简单实验方法是测定吸收塔内溶液的pH。(4)从滤液中得到NaC1O2·3H2O粗晶体的实验操作依次是先将溶液蒸发水分得到NaC1O2的饱和溶液,再降低温度,利用它的溶解度随温度的升高而增大,随温度的降低而减小的特点,冷却结晶,最后过滤即得NaC1O2·3H2O。II.(1)氯碱工业中的原料为饱和食盐水原料需要净化是因为杂质容易堵塞离子交换膜。阳极产品是氯气。阴极产品是氢气和氢氧化钠。(2)工业生产NaC1O3的化学方程式为3Cl2+6NaOH==5NaCl+NaClO3+3H2O 。
考点:考查重要的含氯消毒剂亚氯酸钠(NaC1O2)的制法、氯碱工业的原理及产品的知识。

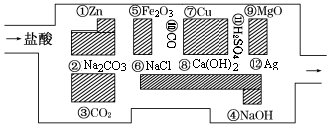
盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题: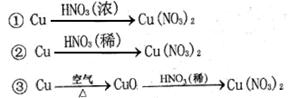
(1) 常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有 性,用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有 性,实验室不能用浓硫酸干燥氨气,说明硫酸具有 性。
(2) 硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。右图所示制备方法符合“绿色化学”思想的
是 (填序号)。
(3) ①在100ml 18 mol/L浓硫酸中加入过量铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是 。
| A.40.32 L | B.30.24 L | C.20.16 L | D.13.44 L |
(4) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水,则反应的化学方程式为 。
 Si3N4 +12HCl
Si3N4 +12HCl