题目内容
【题目】能正确解释下列反应原理,并且其离子方程式书写正确的是( )
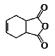
A.泡沫灭火器中Al2(SO4)3和NaHCO3溶液混合:Al3++3HCO![]() =Al(OH)3↓+3CO2↑
=Al(OH)3↓+3CO2↑
B.用小苏打治疗胃酸过多:CO![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
C.电解MgCl2饱和溶液制取Mg:MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
D.用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+
【答案】A
【解析】
A.Al2(SO4)3和NaHCO3溶液混合时,Al3+和HCO![]() 发生双水解生成Al(OH)3和3CO2,离子方程式为Al3++3HCO
发生双水解生成Al(OH)3和3CO2,离子方程式为Al3++3HCO![]() =Al(OH)3↓+3CO2↑,A正确;
=Al(OH)3↓+3CO2↑,A正确;
B.小苏打碳酸氢钠与胃酸发生反应生成氯化钠、二氧化碳和水,离子方程式为HCO![]() +H+=CO2↑+H2O,B错误;
+H+=CO2↑+H2O,B错误;
C.电解MgCl2饱和溶液,水溶液中氢离子优先得电子,无法得到单质镁,C错误;
D.明矾中铝离子水解生成氢氧化铝胶体,不能标记为沉淀,D错误;
答案选A。

【题目】某矿石的主要成分是BaCO3(含Ca2+、Mg2+、Fe3+等杂质)。实验室利用该矿石制备BaCl2·2H2O的流程如图:

(1)用稀盐酸浸取前需充分研磨矿石,目的是__。
(2)加入NH3·H2O调节pH=8可除去__(填离子符号),滤渣Ⅱ中含__(填化学式)。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
(3)要使Ca2+完全沉淀,应控制溶液中的![]() 的浓度不低于__mol/L(离子浓度小于1×10-5mol/L时,认为沉淀就达完全);同时加入H2C2O4时又应避免过量,原因是__。(已知:KSP(BaC2O4=1.6×10-7,KSP(CaC2O4=2.3×10-9)。
的浓度不低于__mol/L(离子浓度小于1×10-5mol/L时,认为沉淀就达完全);同时加入H2C2O4时又应避免过量,原因是__。(已知:KSP(BaC2O4=1.6×10-7,KSP(CaC2O4=2.3×10-9)。
(4)利用氧化还原滴定法可测定H2C2O4的浓度,取20.00mLH2C2O4溶液于锥形瓶中,用0.10mol/L酸性KMnO4溶液滴定,KMnO4溶液应装在__(填“酸式滴定管”或“碱式滴定管”)中。写出反应的离子方程式为__。滴定终点的现象为__。若滴定达到终点时,消耗KMnO4溶液30.00mL,则H2C2O4溶液的浓度为__mol/L。