题目内容
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融) 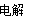 4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融? 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融? 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
A.电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na
B.盖·吕萨克法制钠原理是嫡的增加带动了反应的进行
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1
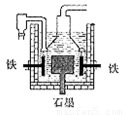
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
【答案】
C
【解析】
试题分析:A、电解池中阴极得到电子发生还原反应,则电解熔融氢氧化钠制钠,阴极发生电极反应为Na++e-=Na,A正确;B、根据反应式3Fe+4NaOH=Fe3O4+4Na↑+2H2↑可知,该反应是熵值增加的反应,因此盖·吕萨克法制钠原理是嫡的增加带动了反应的进行,B正确;C、根据反应方程式可知,若制得1mol钠,则戴维法与盖·吕萨克法中转移电子的物质的量是1mol、2mol,C不正确;D、电解池中阳极失去电子,阴极得到电子,因此用电解熔融氯化钠法制钠时,电解槽中石墨极为阳极,铁为阴极,则D正确,答案选C。
考点:考查电解原理的有关应用与判断

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
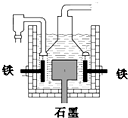 早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法不正确的是( )
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为4NaOH(熔融)═4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH═Fe3O4+2H2↑+4Na↑.下列有关说法不正确的是( )| A、电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-═Na | B、盖?吕萨克法制钠原理是熵的增加带动了反应的进行 | C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1 | D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
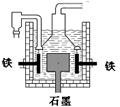 早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔)
早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔)