题目内容
【题目】金属Co、Ni性质相似,在电子工业以及金属材料上应用十分广泛.现以含钴、镍、铝的废渣(含主要成分为CoO、Co2O3、Ni、少量杂质Al2O3)提取钴、镍的工艺如下:
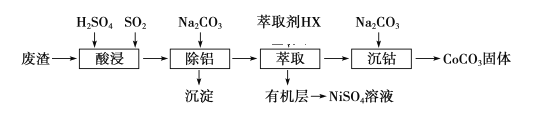
(1)酸浸时SO2的作用是___________________________________。
(2)除铝时加入碳酸钠产生沉淀的离子反应_________________________________。
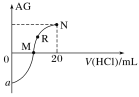
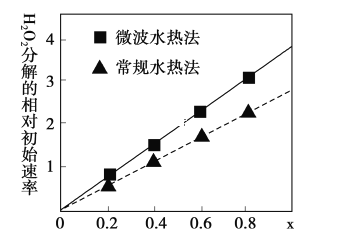
(3)用CoCO3为原料采用微波水热法和常规水热法均可制得H2O2分解的高效催化剂CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价).如图是用两种不同方法制得的CoxNi(1-x)Fe2O4 在10℃时催化分解6%的H2O2 溶液的相对初始速率随x 变化曲线.
①H2O2 的电子式_________________________________。
②由图中信息可知:_________________________________法制取的催化剂活性更高。
③Co2+ 、Ni2+ 两种离子中催化效果更好的是_________________________________。
(4)已知煅烧CoCO3时,温度不同,产物不同.在400℃充分煅烧CoCO3,得到固体氧化物的质量2.41g,CO2的体积为0.672L(标况下),则此时所得固体氧化物的化学式为____________。
【答案】还原剂或将Co3+还原为Co2+ 2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑ ![]() 微波水热 Co2+ Co3O4
微波水热 Co2+ Co3O4
【解析】
第一步酸浸,将氧化物全部变为离子,加入的![]() 具有还原性,可将
具有还原性,可将![]() 还原为
还原为![]() ,第二步加入的碳酸钠,
,第二步加入的碳酸钠,![]() 和
和![]() 可以发生双水解反应,将铝变为沉淀除去,接下来用萃取剂除去镍,此时溶液中只剩下
可以发生双水解反应,将铝变为沉淀除去,接下来用萃取剂除去镍,此时溶液中只剩下![]() ,再加入
,再加入![]() 将
将![]() 转变为
转变为![]() 沉淀即可,本题得解。
沉淀即可,本题得解。
(1)根据分析,![]() 作还原剂;
作还原剂;
(2)根据分析,![]() 和
和![]() 发生双水解反应
发生双水解反应![]() ;
;
(3)①画出过氧化氢的电子式即可![]() ;
;
②根据题图可以看出微波水热法具有更高的反应速率;
③当x增大,催化剂中的![]() 比例增大,
比例增大,![]() 比例减小,而x增大时过氧化氢的分解速率也在增大,说明
比例减小,而x增大时过氧化氢的分解速率也在增大,说明![]() 的催化效果更好;
的催化效果更好;
(4)首先根据![]() 算出
算出![]() 的物质的量,根据碳原子守恒可知碳酸钴的物质的量也为0.03mol,再根据钴原子守恒,2.41g固体中有0.03mol钴原子,剩下的全为氧原子,解得氧原子的物质的量为0.04mol,因此所得固体氧化物的化学式为
的物质的量,根据碳原子守恒可知碳酸钴的物质的量也为0.03mol,再根据钴原子守恒,2.41g固体中有0.03mol钴原子,剩下的全为氧原子,解得氧原子的物质的量为0.04mol,因此所得固体氧化物的化学式为![]() 。
。