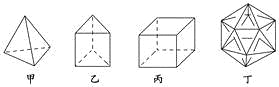
ƒøƒ⁄»ð
°æƒø°ø µ—È “≥£”√—«¡ÚÀ·ƒ∆πÃÃÂ∫Õ70%µƒ≈®¡ÚÀ·÷∆±∏SO2∆¯Ã£¨∑¥”¶∑Ω≥Ã ΩŒ™Na2SO3+H2SO4=Na2SO4+SO2°¸+H2O£¨«Î…˺∆“ªÃ◊ µ—È◊∞÷√£¨ ’ºØ“ª ‘πÐ∏…‘ÔµƒSO2∆¯Ã°£
£®1£©‘⁄œ¬√Ê∑ΩøÚ÷–£¨A±Ì æ”…∑÷“∫¬©∂∑∫Õ◊∂–Œ∆ø◊È≥…µƒ∆¯ÃÂ∑¢…˙∆˜£¨«Î‘⁄¥Ã‚ø®…œµƒA∫ÛÕÍ≥…∏√∑¥”¶µƒ µ—È◊∞÷√ æ“‚Õº(º–≥÷◊∞÷√°¢¡¨Ω”Ω∫πÐ≤ª±ÿª≠≥ˆ£¨Œ≤∆¯¥¶¿Ì≤ø∑÷±ÿ–Ϊ≠≥ˆ£¨–Ë“™º”»»µƒ“«∆˜œ¬∑Ω”√°˜±Í≥ˆ)£¨∞¥∆¯¡˜∑ΩœÚ‘⁄√øº˛“«∆˜œ¬∑Ω±Í≥ˆ◊÷ƒ∏B°¢C°≠£ª∆‰À¸ø…—°”√µƒ“«∆˜( ˝¡ø≤ªœÞ)ºÚ“◊±Ì æ»Áœ¬£∫___

£®2£©∏˘æð∑ΩøÚ÷–µƒ◊∞÷√Õºº◊£¨‘⁄¥Ã‚ø®…œÃÓ–¥œ¬±Ì(ø…≤ªÃÓ¬˙)___
“«∆˜±Í∫≈ | “«∆˜÷–À˘º”ŒÔ÷ | ◊˜”√ |
A | —«¡ÚÀ·ƒ∆°¢≈®¡ÚÀ· | ≤˙…˙SO2 |
£®3£©ƒ≥ µ—È–°◊È”√»ÁÕº““◊∞÷√≤‚∂® ’ºØµΩµƒ∆¯ÃÂ÷–SO2µƒ∫¨¡ø£¨∑¥”¶πÐ÷–◊∞”–À·–‘∏þ√ÕÀ·ºÿ»Ð“∫°£
¢ŸSO2∫ÕÀ·–‘∏þ√ÕÀ·ºÿ»Ð“∫∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™£∫___°£
¢⁄∑¥”¶πЃ⁄»Ð“∫◊œ∫Ï…´œ˚ ß∫Û£¨»Ù√ª”–º∞ ±Õ£÷πÕ®∆¯£¨‘Ú≤‚µ√µƒSO2∫¨¡ø___(—°ÃÓ£∫°∞∆´∏þ°±°¢°∞∆´µÕ°±ªÚ°∞ŒÞ”∞œÏ°±)
¢€»ÙÀ·–‘∏þ√ÕÀ·ºÿ»Ð“∫ê˝Œ™V1mL£¨≈®∂»Œ™cmol/L£¨¡ø∆¯πЃ⁄‘ˆº”µƒÀƵƒÃª˝Œ™V2mL(“—’€À„≥…±Í◊º◊¥øˆœ¬µƒÃª˝)°£”√c°¢V1°¢V2±Ì æSO2µƒÃª˝∞Ÿ∑÷∫¨¡øŒ™___°£
°æ¥∞∏°ø
“«∆˜±Í∫≈ | “«∆˜÷–À˘º”ŒÔ÷ | ◊˜”√ |
A | —«¡ÚÀ·ƒ∆°¢≈®¡ÚÀ· | ≤˙…˙SO2 |
B | ≈®¡ÚÀ· | ≥˝»•ÀÆ’Ù∆¯ |
C | ||
D | «‚—ıªØƒ∆»Ð“∫ | Œ¸ ’π˝¡øµƒ∂˛—ıªØ¡Ú£¨∑¿÷πø’∆¯Œ€»æ |
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ ∆´µÕ ![]() °¡100%
°¡100%
°æΩ‚Œˆ°ø
£®1£©÷∆±∏∆¯Ãµƒ“ª∞„◊∞÷√£∫∑¢…˙◊∞÷√°¢æªªØ◊∞÷√°¢ ’ºØ◊∞÷√£¨æð¥ÀΩ‚¥£ª
£®2£©“¿æð…˺∆≤Ω÷Ë∫Õ ‘º¡—°‘Ò”√—«¡ÚÀ·ƒ∆”Î≈®¡ÚÀ·÷∆±∏¥ø檰¢∏…‘Ôµƒ∂˛—ıªØ¡Ú£¨–Ë“™‘⁄◊∞÷√A÷–º”»Î—«¡ÚÀ·ƒ∆£¨∑÷“∫¬©∂∑÷–º”»Î≈®¡ÚÀ·£¨∂˛—ıªØ¡Ú÷–∫¨”–ÀÆ’Ù∆¯£¨Õ®π˝≈®¡ÚÀ·≥˝»•ÀÆ’Ù∆¯£¨‘⁄ºØ∆¯∆ø÷– ’ºØ¥øæª∏…‘Ôµƒ¬»∆¯£¨◊Ó∫Û”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’∂˛—ıªØ¡Ú∑¿÷πŒ€»æø’∆¯£ª
£®3£©¢Ÿ∏þ√ÃÀ·∏˘¿Î◊”‘⁄À·–‘ª∑æ≥œ¬æþ”–«øµƒ—ıªØ–‘£¨ƒÐπª—ıªØ∂˛—ıªØ¡Ú…˙≥…¡ÚÀ·∏˘¿Î◊”£ª
¢⁄∑¥”¶πЃ⁄»Ð“∫◊œ∫Ï…´œ˚ ß ±£¨SO2”Î∑¥”¶πЃ⁄À˘∫¨µƒ∏þ√ÃÀ·∏˘¿Î◊”«°∫√∑¥”¶£¨»Ù√ªº∞ ±Õ£÷πÕ®∆¯£¨‘ÚŒ¥∑¥”¶µƒSO2∆¯Ã“≤≈≈ÀÆµΩ¡ø∆¯πУª
¢€∏˘æð∑¥”¶£∫5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+£¨n£®SO2£©=2.5V1c°¡10-3mol£¨“¿æðV=Vmnº∆À„∂˛—ıªØ¡ÚµƒÃª˝£¨»ª∫Ûº∆À„∂˛—ıªØ¡Úµƒ∞Ÿ∑÷∫¨¡ø°£
![]() ÷∆±∏∆¯Ãµƒ“ª∞„◊∞÷√£∫∑¢…˙◊∞÷√°¢æªªØ◊∞÷√°¢ ’ºØ◊∞÷√£¨“¿æð∑¥”¶∑Ω≥à Ω
÷∆±∏∆¯Ãµƒ“ª∞„◊∞÷√£∫∑¢…˙◊∞÷√°¢æªªØ◊∞÷√°¢ ’ºØ◊∞÷√£¨“¿æð∑¥”¶∑Ω≥à Ω![]() £¨÷∆±∏∏…‘Ôµƒ∂˛—ıªØ¡Ú–Ë“™‘⁄A÷–º”»Î—«¡ÚÀ·ƒ∆πÃã¨∑÷“∫¬©∂∑÷–º”»Î≈®¡ÚÀ·£¨º”»»∑¥”¶…˙≥…∂˛—ıªØ¡Ú£¨∂˛—ıªØ¡Ú÷–∫¨”–ÀÆ’Ù∆¯£¨–Ë“™Õ®π˝≈®¡ÚÀ·≥˝»•ÀÆ’Ù∆¯£¨‘⁄ºØ∆¯∆ø÷–”√œÚ…œ≈≈ø’∆¯∑® ’ºØ ’ºØ¥øæª∏…‘Ôµƒ∂˛—ıªØ¡Ú£¨◊Ó∫Û”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’π˝¡øµƒ∂˛—ıªØ¡Ú∑¿÷πŒ€»æø’£¨◊∞÷√»ÁÕº
£¨÷∆±∏∏…‘Ôµƒ∂˛—ıªØ¡Ú–Ë“™‘⁄A÷–º”»Î—«¡ÚÀ·ƒ∆πÃã¨∑÷“∫¬©∂∑÷–º”»Î≈®¡ÚÀ·£¨º”»»∑¥”¶…˙≥…∂˛—ıªØ¡Ú£¨∂˛—ıªØ¡Ú÷–∫¨”–ÀÆ’Ù∆¯£¨–Ë“™Õ®π˝≈®¡ÚÀ·≥˝»•ÀÆ’Ù∆¯£¨‘⁄ºØ∆¯∆ø÷–”√œÚ…œ≈≈ø’∆¯∑® ’ºØ ’ºØ¥øæª∏…‘Ôµƒ∂˛—ıªØ¡Ú£¨◊Ó∫Û”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’π˝¡øµƒ∂˛—ıªØ¡Ú∑¿÷πŒ€»æø’£¨◊∞÷√»ÁÕº £ª
£ª
![]() “¿æð…˺∆≤Ω÷Ë∫Õ ‘º¡—°‘Ò”√—«¡ÚÀ·ƒ∆”Î≈®¡ÚÀ·÷∆±∏¥ø檰¢∏…‘Ôµƒ∂˛—ıªØ¡Ú£¨–Ë“™‘⁄◊∞÷√A÷–º”»Î—«¡ÚÀ·ƒ∆£¨∑÷“∫¬©∂∑÷–º”»Î≈®¡ÚÀ·£¨∂˛—ıªØ¡Ú÷–∫¨”–ÀÆ’Ù∆¯£¨Õ®π˝≈®¡ÚÀ·≥˝»•ÀÆ’Ù∆¯£¨‘⁄ºØ∆¯∆ø÷– ’ºØ¥øæª∏…‘Ôµƒ¬»∆¯£¨◊Ó∫Û”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’∂˛—ıªØ¡Ú∑¿÷πŒ€»æø’∆¯£ªÃÓ–¥±Ì∏ÒŒ™£∫
“¿æð…˺∆≤Ω÷Ë∫Õ ‘º¡—°‘Ò”√—«¡ÚÀ·ƒ∆”Î≈®¡ÚÀ·÷∆±∏¥ø檰¢∏…‘Ôµƒ∂˛—ıªØ¡Ú£¨–Ë“™‘⁄◊∞÷√A÷–º”»Î—«¡ÚÀ·ƒ∆£¨∑÷“∫¬©∂∑÷–º”»Î≈®¡ÚÀ·£¨∂˛—ıªØ¡Ú÷–∫¨”–ÀÆ’Ù∆¯£¨Õ®π˝≈®¡ÚÀ·≥˝»•ÀÆ’Ù∆¯£¨‘⁄ºØ∆¯∆ø÷– ’ºØ¥øæª∏…‘Ôµƒ¬»∆¯£¨◊Ó∫Û”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’∂˛—ıªØ¡Ú∑¿÷πŒ€»æø’∆¯£ªÃÓ–¥±Ì∏ÒŒ™£∫
“«∆˜±Í∫≈ | “«∆˜÷–À˘º”ŒÔ÷ | ◊˜”√ |
A | —«¡ÚÀ·ƒ∆°¢≈®¡ÚÀ· | ≤˙…˙ |
B | ≈®¡ÚÀ· | ≥˝»•ÀÆ’Ù∆¯ |
C | ||
D | «‚—ıªØƒ∆»Ð“∫ | Œ¸ ’π˝¡øµƒ∂˛—ıªØ¡Ú£¨∑¿÷πø’∆¯Œ€»æ |
![]() ∏þ√ÃÀ·∏˘¿Î◊”‘⁄À·–‘ª∑æ≥œ¬æþ”–«øµƒ—ıªØ–‘£¨ƒÐπª—ıªØ∂˛—ıªØ¡Ú…˙≥…¡ÚÀ·∏˘¿Î◊”£¨∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «
∏þ√ÃÀ·∏˘¿Î◊”‘⁄À·–‘ª∑æ≥œ¬æþ”–«øµƒ—ıªØ–‘£¨ƒÐπª—ıªØ∂˛—ıªØ¡Ú…˙≥…¡ÚÀ·∏˘¿Î◊”£¨∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «![]() £ª
£ª
![]() ∑¥”¶πЃ⁄»Ð“∫◊œ∫Ï…´œ˚ ß∫Û£¨»Ù√ª”–º∞ ±Õ£÷πÕ®∆¯£¨æÕª· πµ√
∑¥”¶πЃ⁄»Ð“∫◊œ∫Ï…´œ˚ ß∫Û£¨»Ù√ª”–º∞ ±Õ£÷πÕ®∆¯£¨æÕª· πµ√![]() ªÏ∫œ∆¯ÃÂ
ªÏ∫œ∆¯ÃÂ![]() ‘ˆ¥Û£¨‘Ú∂˛—ıªØ¡Úµƒ∫¨¡ø∆´µÕ£ª
‘ˆ¥Û£¨‘Ú∂˛—ıªØ¡Úµƒ∫¨¡ø∆´µÕ£ª
![]() ∏˘æð∑¥”¶£∫
∏˘æð∑¥”¶£∫![]() £¨
£¨![]() £¨∆‰±Íøˆœ¬Ãª˝
£¨∆‰±Íøˆœ¬Ãª˝![]() £¨º¥
£¨º¥![]() £ªÀ˘“‘
£ªÀ˘“‘![]() µƒÃª˝∞Ÿ∑÷∫¨¡øŒ™
µƒÃª˝∞Ÿ∑÷∫¨¡øŒ™![]() °£
°£

 ’„Ω≠√˚–£√˚ ¶ΩæÌœµ¡–¥∞∏
’„Ω≠√˚–£√˚ ¶ΩæÌœµ¡–¥∞∏°æƒø°øΩÒ”– “Œ¬œ¬Àƒ÷÷»Ð“∫£¨”–πÿ– ˆ≤ª’˝»∑µƒ «
–Ú∫≈ | ¢Ÿ | ¢⁄ | ¢€ | ¢Ð |
pH | 11 | 11 | 3 | 3 |
»Ð“∫ | ∞±ÀÆ | «‚—ıªØƒ∆»Ð“∫ | ¥◊À· | —ŒÀ· |
A. ¢€¢Ð÷–∑÷±º”»Î ¡øµƒ¥◊À·ƒ∆æßÃÂ∫Û£¨¡Ω»Ð“∫µƒpHæ˘‘ˆ¥Û
B. ¢⁄¢€¡Ω»Ð“∫µ»Ãª˝ªÏ∫œ£¨À˘µ√»Ð“∫÷–c(H£´)£æc(OH£≠)
C. ∑÷±º”ÀÆœ° Õ10±∂£¨Àƒ÷÷»Ð“∫µƒpH¢Ÿ£æ¢⁄£æ¢Ð£æ¢€
D. V1L¢Ð”ÎV2L¢Ÿ»Ð“∫ªÏ∫œ∫Û£¨»ÙªÏ∫œ∫ۻГ∫pH£Ω7£¨‘ÚV1£ºV2